Nung m gam bột Cu trong oxi thu được 24,8 gam hỗn hợp chất rắn X gồm Cu, CuO, Cu2O. Hoà tan hoàn toàn X bằng H2SO4 đặc, nóng thu được 4,48 lít (đktc) khí SO2 duy nhất. Giá trị m là:
A. 9,68gam.
B. 15,84 gam.
C. 20,32 gam.
D. 22,4gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
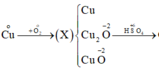
![]()
mX = 64x + 32y = 24,8 (1)
Bảo toàn e: nelectron cho = nelectron nhận
![]()
=> 2x = 4y + 0,2.2 (2)
=> x = 0,
35 và y = 0,075 m = 0,35.64 = 22,4 gam.

Cu + O2 → hỗn hợp rắn X
Theo ĐL Bảo toàn khối lượng có mO2= 24,8-m (gam)
→ nO2= (24,8-m)/32 mol
Ta có nNO2= 0,4 mol
QT cho e:
Cu→ Cu2++ 2e
m/64 2m/64 mol
QT nhận e :
O2+ 4e→ 2O-2
(24,8-m)/32 (24,8-m)/8
N+5+ 1e → NO2
0,4←0,4
Theo ĐL BT electron thì : ne cho= ne nhận
Nên 2m/64= (24,8-m)/8+ 0,4 Suy ra m= 22,4 gam
Đáp án D

Quy đổi hỗn hợp X : Cu: a mol, O: b mol
⇒ 64a+16b=35,6 (1)
nSO2=\(\dfrac{6,72}{22,4}=0,3\) mol
Cu→Cu2+ + 2e
a → 2a
O + 2e → O2-
b → 2b
S6+ + 2e → S4+
0,6 ← 0,3
Bte: 2a - 2b=0,6 (2)
Từ (1), (2) ⇒\(\left\{{}\begin{matrix}a=0,505\\b=0,205\end{matrix}\right.\)
⇒ m= 0,505 . 64 = 32,32g
Quy đổi hh gồm Cu (a mol) và O (b mol)
Theo bài ra: \(64a+16b=35,6\) (1)
Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Bảo toàn electron: \(2n_{Cu}=2n_O+2n_{SO_2}\) \(\Rightarrow2a-2b=0,6\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,505\\b=0,205\end{matrix}\right.\)
\(\Rightarrow m_{Cu}=0,505\cdot64=32,32\left(g\right)\)
\(\Rightarrow\) Đáp án B
Chọn D.