Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Số mol SO2 thu được là: n SO 2 = 11 , 2 22 , 4 = 0 , 5 mol
Sơ đồ phản ứng:
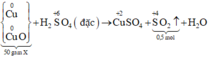
Các quá trình nhường , nhận electron:
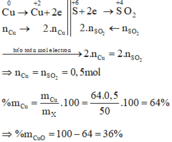

Khí thoát ra : NO2
Coi hỗn hợp X gồm Fe,O
Ta có :
\(n_{Fe} = \dfrac{7,28}{56} =0,13(mol) ; n_{NO_2} = \dfrac{1,568}{22,4} =0,07(mol)\)
Bảo toàn e :
\(3n_{Fe} = 2n_O + n_{NO_2}\Rightarrow n_O = \dfrac{0,13.3-0,07}{2} =0,16 \ mol\)
Suy ra : \(m_X = m_{Fe} + m_O = 7,28 + 0,16.16 = 9,84(gam)\)

Đáp án C
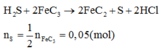
Chú ý: Không tồn tại muối sunfua của Al và Fe(III). H2S không phản ứng với AlCl3 nhưng nếu
![]()
Có sự khác nhau này do Fe3+ có tính oxi hóa mạnh còn Al3+ tính oxi hóa yếu
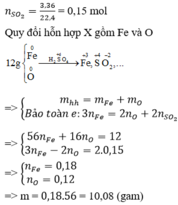
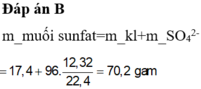
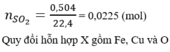
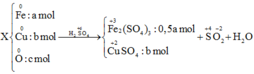
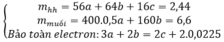
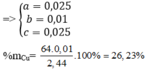




Quy đổi hỗn hợp X : Cu: a mol, O: b mol
⇒ 64a+16b=35,6 (1)
nSO2=\(\dfrac{6,72}{22,4}=0,3\) mol
Cu→Cu2+ + 2e
a → 2a
O + 2e → O2-
b → 2b
S6+ + 2e → S4+
0,6 ← 0,3
Bte: 2a - 2b=0,6 (2)
Từ (1), (2) ⇒\(\left\{{}\begin{matrix}a=0,505\\b=0,205\end{matrix}\right.\)
⇒ m= 0,505 . 64 = 32,32g
Quy đổi hh gồm Cu (a mol) và O (b mol)
Theo bài ra: \(64a+16b=35,6\) (1)
Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Bảo toàn electron: \(2n_{Cu}=2n_O+2n_{SO_2}\) \(\Rightarrow2a-2b=0,6\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,505\\b=0,205\end{matrix}\right.\)
\(\Rightarrow m_{Cu}=0,505\cdot64=32,32\left(g\right)\)
\(\Rightarrow\) Đáp án B