Cho 23,2 gam Fe3O4 tác dụng với dung dịch HCl dư thu được muối sắt có khối lượng là:
A. 48,6gam
B. 28,9gam
C. 45,2g
D. 25,4g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(b,n_{Fe}=\dfrac{50,4}{56}=0,9(mol)\\ PTHH:3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ \Rightarrow n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,3(mol)\\ \Rightarrow m_{Fe_3O_4}=0,3.232=69,6(g)\\ c,PTHH:Fe_3O_4+8HCl\xrightarrow{t^o}FeCl_2+2FeCl_3+4H_2O\\ \Rightarrow n_{FeCl_2}=0,3(mol);n_{FeCl_3}=0,6(mol)\\ \Rightarrow m_{\text {muối}}=m_{FeCl_2}+m_{FeCl_3}=0,3.127+0,6.162,5=135,6(g)\)

$n_{HCl}=0,2.2=0,4(mol)$
BTNT(H): $n_{H_2O}=0,5n_{HCl}=0,2(mol)$
BTNT(O): $n_{O(\text{trong oxit})}=n_{H_2O}=0,2(mol)$
$\to m_X=0,2.16+20=23,2(g)$
$\to A$
\(m_{rắn}=m_{kl}+m_O\\ n_{HCl}=0,2.2=0,4\left(mol\right)\Rightarrow n_O=n_{H_2O}=\dfrac{n_{HCl}}{2}=\dfrac{0,4}{2}=0,2\left(mol\right)\\ m_{rắn}=20+0,2.16=23,2\left(g\right)\\ \Rightarrow Chọn.A\)

a. Ta có: \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
Ta lại có: \(C_{\%_{HCl}}=\dfrac{m_{ct_{HCl}}}{100}.100\%=7,3\%\)
=> mHCl = 7,3(g)
=> \(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
PTHH:
Fe3O4 + 8HCl ---> FeCl2 + 2FeCl3 + 4H2O
1 ---> 8
0,1 ---> 0,2
=> \(\dfrac{0,1}{1}>\dfrac{0,2}{8}\)
Vậy Fe3O4 dư
=> mdư = 23,2 - 7,3 = 15,9 (g)
b. Theo PT: \(n_{FeCl_2}=\dfrac{1}{8}.n_{HCl}=\dfrac{1}{8}.0,2=0,025\left(mol\right)\)
=> \(m_{FeCl_2}=0,025.127=3,175\left(g\right)\)
Theo PT: \(n_{FeCl_3}=\dfrac{1}{4}.n_{HCl}=\dfrac{1}{4}.0,2=0,05\left(mol\right)\)
=> \(m_{FeCl_3}=0,05.162,5=8,125\left(g\right)\)
=> \(m_{muối}=8,125+3,175=11,3\left(g\right)\)
c. Ta có: mdung dịch sau PỨ = \(23,2+100=123,2\left(g\right)\)
Theo PT: \(n_{H_2O}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{H_2O}=0,1.18=1,8\left(g\right)\)
mcác chất sau PỨ = 1,8 + 11,3 = 13,1(g)
=> \(C_{\%_{sauPỨ}}=\dfrac{13,1}{123,2}.100\%=10,63\%\)

PTHH: \(Fe_3O_4+8HCl\rightarrow FeCl_2+2FeCl_3+4H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\\n_{HCl}=\dfrac{300\cdot3,65\%}{36,5}=0,3\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,3}{8}\) \(\Rightarrow\) Fe3O4 còn dư, HCl p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_3O_4\left(dư\right)}=0,0625\left(mol\right)\\n_{FeCl_2}=0,0375\left(mol\right)\\m_{FeCl_3}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_3O_4\left(dư\right)}=0,0625\cdot232=14,5\left(g\right)\\m_{muối}=0,0375\cdot127+0,075\cdot162,5=16,95\left(g\right)\end{matrix}\right.\)
nFe3O4= 23,2/232=0,1(mol); nHCl = (300.3,65%)/36,5= 0,3(mol)
a) PTHH: Fe3O4 + 8 HCl -> 2 FeCl3 + FeCl2 + 4 H2O
b) Ta có: 0,3/8 < 0,1/1
=> Fe3O4 dư, HCl hết, tính theo nHCl.
=> nFe3O4(p.ứ)= nFeCl2= nHCl/8=0,3/8= 0,0375(mol)
=> mFe3O4(dư)= (0,1- 0,0375).232=14,5(g)
c) nFeCl3= 2/8. 0,3= 0,075(mol)
=> mFeCl3= 0,075.162,5=12,1875(g)
mFeCl2= 0,0375. 127=4,7625(g)
=>m(muối)= 12,1875+ 4,7625= 16,95(g)

nFe3O4= 23,2/232=0,1(mol)
nH2SO4=2.0,25=0,5(mol)
a) PTHH: Fe3O4 + 4 H2SO4 -> Fe2(SO4)3 + FeSO4 + 4 H2O
Ta có: 0,1/1 < 0,5/4
=> H2SO4 dư, Fe3O4 hết, tính theo Fe3O4
nFe2(SO4)3=nFeSO4=nFe3O4=0,1(mol)
=> mFe2(SO4)3=0,1.400=40(g)
mFeSO4=0,1.152=15,2(g)
b) nH2SO4(dư) = 0,5- 0,1.4=0,1(mol)
Vddsau=VddH2SO4=0,25(l)
=> CMddH2SO4(dư)=CMddFe2(SO4)3=CMddFeSO4=0,1/0,25=0,4(M)

Đáp án A
nFe = 0,05 (mol)
Fe + 2HCl → FeCl2 + H2
0,05 → 0,05
=> ![]()
2Fe +3Cl2 → 2FeCl3
0,05 0,05
=> ![]()
mMuối = 6,35 + 8,125 = 14,475 (g)

Quy đổi hỗn hợp B gồm Fe (x mol) và O (y mol)
Ta có: \(56x+16y=21,6\) (1)
Bảo toàn electron: \(3x=2y+3n_{NO}=2y+0,3\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,3\end{matrix}\right.\) \(\Rightarrow m_{Fe}=0,3\cdot56=16,8\left(g\right)\)

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
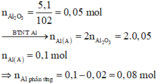
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
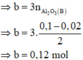
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
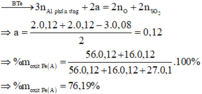
Đáp án C
nFe3O4 = 23,2: 232 = 0,1 mol
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
Mol 0,1 → 0,1 → 0,2
mmuối = mFeCl2 + mFeCl3 = 0,1.127 + 0,2.162,5 = 45,2g