Cho 1,3 gam kẽm phản ứng với 14,7 gam dung dịch H 2 SO 4 20%. Khi phản ứng kết thúc khối lượng khí thoát ra là:
A. 0,03 gam
B. 0,06 gam
C. 0,04 gam
D. 0,02 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Z n + H 2 S O 4 → Z n S O 4 + H 2
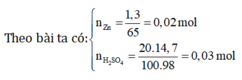 ⇒ Zn phản ứng hết, dd axit còn dư
⇒ Zn phản ứng hết, dd axit còn dư
⇒ n H 2 = n Z n = 0,02 mol
⇒ m H 2 = 2.0,02 = 0,04 g
⇒ Chọn C.

\(m_{ct}=\dfrac{20.14,7}{100}=2,94\left(g\right)\)
\(n_{H2SO4}=\dfrac{2,94}{98}=0,03\left(mol\right)\)
Pt : \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,03 0,03 0,03
\(n_{Zn}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
⇒ \(m_{Zn}=0,03.65=1,95\left(g\right)\)
\(n_{H2}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,03.22,4=0,672\left(l\right)\)
⇒ Chọn câu : D
Chúc bạn học tốt

Định hướng tư duy giải
Ta có:
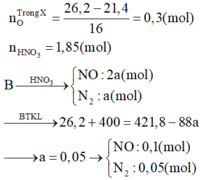

Chất tan trong bình gồm hỗn hợp muối và HNO3 dư.
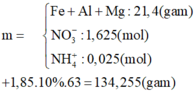

Dạng bài toán cho kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối của chúng có hai trường hợp sau
+ Nếu đề bài cho khối lượng thanh kim loại tăng, lập phương trình đại số :
m kim loại giải phóng - m kim loại tan = m kim loại tăng
+ Nếu đề bài cho khối lượng thanh kim loại giảm, lập phương trình đại số :
m kim loại tan - m kim loại giải phóng = m kim loại giảm
Gọi x là số mol Zn tham gia
65x - 64x = 25 - 24,96 => x = 0,04 mol
m Zn p / u = 0,04 x 65 = 2,6 g

\(n_{Zn}=\dfrac{1,3}{65}=0,02\left(mol\right)\\
pthhZn+2HCl\rightarrow ZnCl_2+H_2\)
0,02 0,02 0,02
\(m_{ZnCl_2}=136.0,02=2,72\left(g\right)\\
V_{H_2}=0,02.22,4=0,448\left(l\right)\)