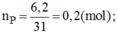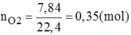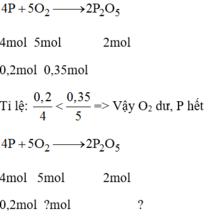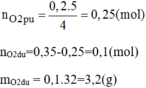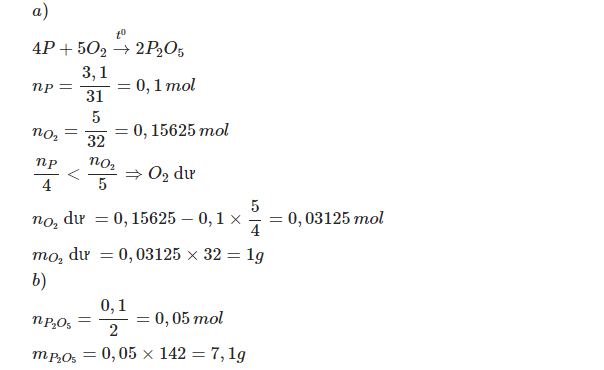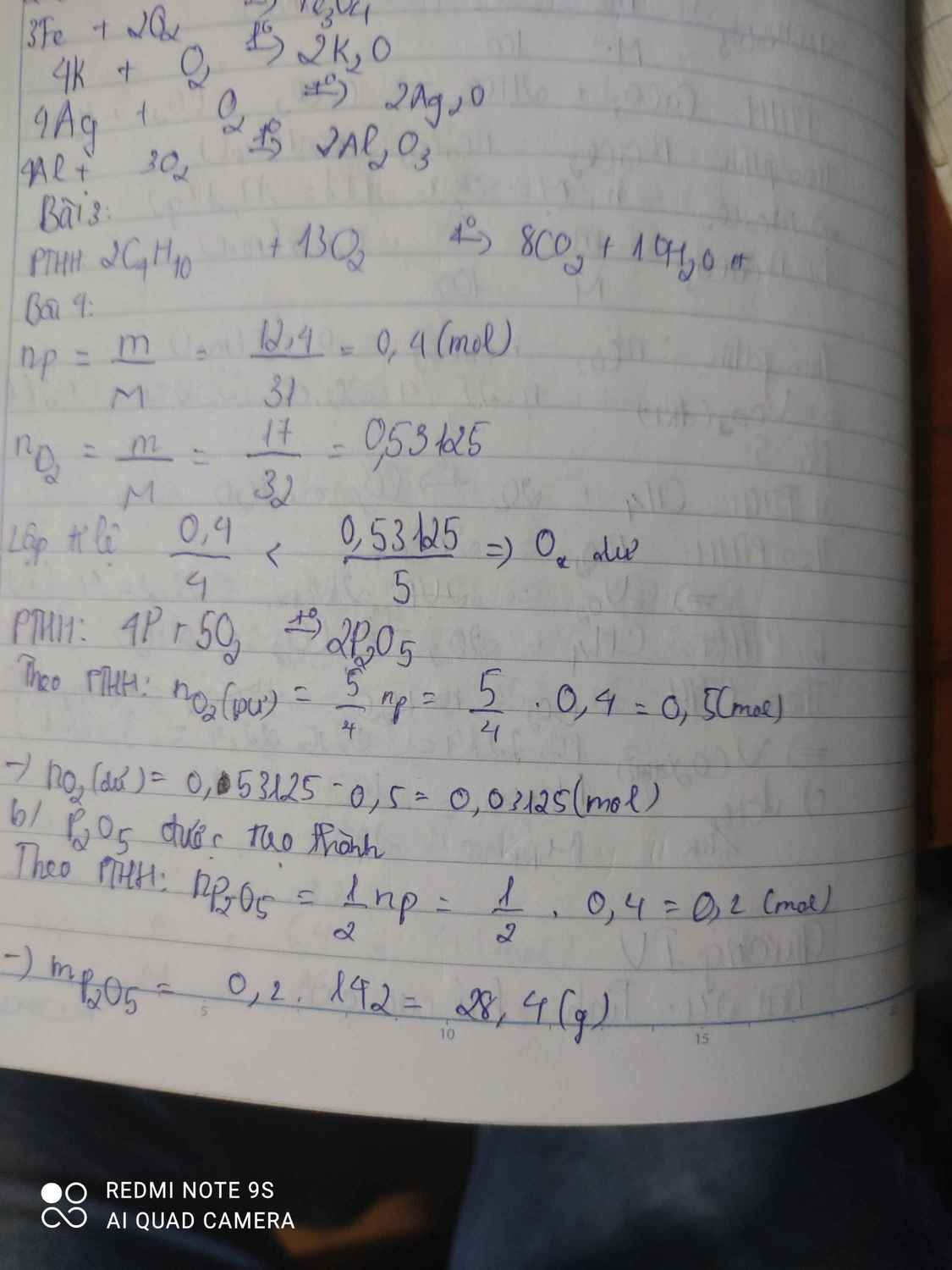Đốt cháy 6,2g photpho trong bình chứa 7,84 lit oxi (đktc). Hãy cho biết sau khi cháy: Chất nào được tạo thành và khối lượng là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

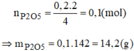

\(n_P=\dfrac{m}{M}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PTHH:\(4P+5O_2\rightarrow2P_2O_5\)
tpứ: 0,2 0,35
pứ: 0,2 0,25 0,1
spứ: 0 0,1 0,1
a)chất còn dư là oxi
\(m_{O_2dư}=n.M\)=0,1.32=3,2(g)
b)\(m_{P_2O_5}=n.M\)=0,1.142=14,2(g)

\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(n_{O_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
\(4P+5O_2\underrightarrow{^{^{t^0}}}2P_2O_5\)
\(4........5\)
\(0.2........0.35\)
\(LTL:\dfrac{0.2}{4}< \dfrac{0.35}{5}\Rightarrow O_2dư\)
\(m_{O_2\left(dư\right)}=\left(0.35-0.25\right)\cdot32=3.2\left(g\right)\)
\(m_{P_2O_5}=0.1\cdot142=14.2\left(g\right)\)
Tham khảo nha!!!
nP = 6,2/31 = 0,2 mol ; nO2 = 7,84/22,4 = 0,35 mol
a, PTHH : 4P + 5O2 (to) -> 2P2O5
0,2 0,35 mol
Ta thấy : 0,2/4 < 0,35/5 -> nO2 dư = 0,35 - 0,05*5 = 0,1 mol
-> mO2 dư = 0,1*32 = 3,2 gam
b, Theo pt : nP2O5 = 1/2*nP = 0,1 mol -> mP2O5 = 0,1*142 = 14,2 gam

a. \(n_{Mg}=\dfrac{m}{M}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: \(2Mg+O_2\rightarrow^{t^0}2MgO\)
-Theo PTHH: 2 1 2 (mol)
-Theo đề bài: 0,2 0,1 (mol)
-So sánh tỉ lệ số mol đề bài với số mol phương trình của Mg và O2 có:
\(\dfrac{0,2}{2}=\dfrac{0,1}{1}\)
\(\Rightarrow\) Mg và O2 phản ứng hết.
b. -Chất tạo thành: Magie oxit.
\(n_{MgO}=\dfrac{0,1.2}{1}=0,2\) (mol)
\(\Rightarrow m_{MgO}=n.M=0,2.40=8\left(g\right)\)

\(a) n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ \dfrac{n_P}{4} = 0,05 < \dfrac{n_{O_2}}{5}=0,06 \to O_2\ dư\\ n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)\\ m_{O_2\ dư} = (0,3 - 0,25).32 = 1,6(gam)\\ b) P_2O_5\ \text{được tạo thành}\\ n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ m_{P_2O_5} = 0,1.142 = 14,2(gam)\)

ta có : nP=9,3:31=0,3 mol
nO=5,6:22,4=0,25 mol
PTHH: 5O2 + 2P\(\rightarrow\) 2P2O5
ban đầu: 0,25 0,3 (mol)
phản ứng: 0,25 \(\rightarrow\) 0,25 (mol)
sau phản ứng: 0 0,05 0,1 (mol)
vậy sau phản ứng O2 hết còn P dư
mP dư= 0,05.31=1,55 g
b) chất P2O5
mP2O5= 0,1.390=39 g

\(n_P=\dfrac{m_p}{M_P}=\dfrac{12,4}{31}=0,4mol\)
\(n_{O_2}=\dfrac{m_{O_2}}{M_{O_2}}=\dfrac{17}{32}=0,53125mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
4 5 2 ( mol )
0,4 0,53125 ( mol )
ta có: \(\dfrac{0,4}{4}< \dfrac{0,53125}{5}\)
=> Chất dư là \(O_2\)
\(n_{O_2\left(du\right)}=0,53125-0,5=0,03125mol\)
Chất được tạo thành là \(P_2O_5\)
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=\left(\dfrac{0,4.2}{4}\right).142=28,4g\)