Tính chất hóa học đặc trưng của
A. metan là phản ứng thế, và etilen là phản ứng cộng
B. metan và etilen là phản ứng thế
C. metan và etilen là phản ứng cộng
D. metan và etilen là phản ứng cháy
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(CH_4+Cl_2\xrightarrow[]{a/s}CH_3Cl+HCl\\ CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\\ CH\equiv CH+2Br_2\rightarrow CHBr_2-CHBr_2\\ CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\\ C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\\ 2C_2H_2+5O_2\xrightarrow[]{t^o}4CO_2+2H_2O\\ nCH_2=CH_2\xrightarrow[]{t^o,p,xt}\left(-CH_2-CH_2-\right)_n\)

Bài 2:
_ Dẫn hỗn hợp khí qua bình đựng nước vôi trong.
+ Nếu xuất hiện kết tủa trắng, đó là CO2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
+ Nếu không có hiện tượng, đó là CH4 và C2H4. (1)
_ Dẫn hỗn hợp khí nhóm (1) qua bình đưng nước brom dư.
+ Nếu nước brom nhạt màu, đó là C2H4.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
+ Nếu không có hiện tượng, đó là C2H4.
Bài 5:
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(n_{C_2H_4Br_2}=\dfrac{18,8}{188}=0,1\left(mol\right)\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,1\left(mol\right)\)
\(\Rightarrow V_{C_2H_4}=0,1.22,4=2,24\left(l\right)\)
\(\Rightarrow V_{CH_4}=5,6-2,24=3,36\left(l\right)\)
c, Ta có: \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{2,24}{5,6}.100\%=40\%\\\%V_{CH_4}=60\%\end{matrix}\right.\)
Bài 6: Phần này mình sửa thành 37,6 g cho số mol đẹp nhé!
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(n_{C_2H_4Br_2}=\dfrac{37,6}{188}=0,2\left(mol\right)\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{C_2H_4}=0,2.22,5=4,48\left(l\right)\)
\(\Rightarrow V_{CH_4}=11,2-4,48=6,72\left(l\right)\)
c, Ta có: \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{4,48}{11,2}.100\%=40\%\\\%V_{CH_4}=60\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Câu 3.
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(n_{Br_2}=\dfrac{4,2}{160}=0,02625mol\)
\(\Rightarrow n_{etilen}=0,02625mol\Rightarrow n_{metan}=0,22375mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(\%V_{C_2H_4}=\dfrac{0,02625}{0,25}=10,5\%\)
\(\%V_{CH_4}=100\%-10,5\%=89,5\%\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(\Rightarrow\Sigma n_{O_2}=2\cdot0,22375+3\cdot0,02625=0,52625\)
\(\Rightarrow V_{O_2}=11,788l\)

Phát biểu đúng: b). Vậy số phát biểu đúng là 1
Các phát biểu sai là:
a) Metan cháy với oxi tạo hơi nước và khí lưu huỳnh đioxit => Sai vì tạo khí cacbonic ( C O 2 ) chứ không phải là lưu huỳnh đioxit
c) Trong phản ứng hóa học giữa Metan và Clo, chỉ có duy nhất một nguyên tử Hiđro của Metan có thể được thay thế bởi nguyên tử Clo => Sai.
d) Hỗn hợp gồm hai thể tích Metan và một thể tích Oxi là hỗn hợp nổ mạnh => Sai, hỗn hợp nổ gồm một thể tích Metan và hai phần thể tích Oxi
Đáp án: A

Tính chất hoá học của Metan CH4
1. Metan tác dụng với oxi:
- Khi đốt trong oxi, metan cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
CH4 + 2O2 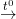 CO2 + 2H2O
CO2 + 2H2O
2. Metan tác dụng với clo khi có ánh sáng
CH4 + Cl2 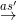 HCl + CH3Cl (metyl clorua)
HCl + CH3Cl (metyl clorua)
- Ở phản ứng này, nguyên tử H của metan được thay thế bởi nguyên tử Cl, vì vậy còn được gọi là phản ứng thế.
Tính chất hoá học của etilen C2H4
1) Etilen C2H4 Tác dụng với oxi:
- Khi đốt trong oxi, etilen cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
C2H4 + 3O2 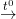 2CO2↑ + 2H2O
2CO2↑ + 2H2O
2) Etilen C2H4 tác dụng với dung dịch Brom
- Dung dịch Brom hay nước Brom có màu vàng da cam; Ở phản ứng này, một liên kết kém bền trong liên kết dôi bị đứt ra và phân tử etilen kết hợp thêm một phân tử brom. Phản ứng trên gọi là .hàn ứng cộng.
CH2=CH2 + Br2 (dd) → Br-CH2-CH2-Br
- Ngoài Brom, trong những điều kiện thích hợp, etilen còn có phản ứng cộng vởi một số chất khác, như hiđro,...
3. Phản ứng trùng hợp của etilen C2H4
- Khi có xúc tác và nhiệt độ thích hợp, liên kết kém bền trong phân tử etilen bị dứt ra làm cho các phân tử etilen kết hợp với nhau, tạo thành chất có phân tử lượng rất lớn gọi là polime.
...+ CH2=CH2 + CH2=CH2 + CH2=CH2 + ... ![small xrightarrow[t^{0},P]{xt}](https://hayhochoi.vn/uploads/news/wyswyg/2019_01/giflatexsmallspacexrightarrowt0p_1548216818.gif) ...- CH2- CH2- CH2- CH2- CH2- CH2-...
...- CH2- CH2- CH2- CH2- CH2- CH2-...
- Phản ứng trên được gọi là phản ứng trùng hợp, polietilen (PE) là chất rắn, không độc, không tan trong nước và là nguyên liệu quan trọng trong công nghiệp chất dẻo.
Tính chất hoá học của Axetilen (C2H2)
1. Axetilen tác dụng với Oxi
- Khi đốt trong không khí, axetilen cháy với ngọn lửa sáng, tỏa nhiều nhiệt
2C2H2 + 5O2 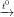 4CO2↑ + 2H2O
4CO2↑ + 2H2O
2. Axetilen tác dụng với dung dịch brom
- Trong liên kết ba  của phân tử axetilen có 2 liên kết kém bền, vì vậy axetilen cũng làm mất màu dung dịch brom như etilen theo PTPƯ sau:
của phân tử axetilen có 2 liên kết kém bền, vì vậy axetilen cũng làm mất màu dung dịch brom như etilen theo PTPƯ sau:
HC CH + Br2 —> Br-CH=CH—Br (đibrom etilen)
CH + Br2 —> Br-CH=CH—Br (đibrom etilen)
Br-CH=CH-Br + Br2 —> Br2CH-CHBr2 (tetra brometan)
- Nếu nước brom lấy dư và axetilen phản ứng hết:
HC CH + 2Br2 —> Br2CH-CHBr2
CH + 2Br2 —> Br2CH-CHBr2
- Trong điều kiện thích hợp, axetilen còn tham gia phản ứng cộng với nhiều chất khác như H2, Cl2,...
| Metan | Etilen | Axetilen | Benzen | |
| Công thức cấu tạo |  |  |  |  |
| Đặc điểm cấu tạo | Có 4 liên kết đơn σ giữa C và H | Có 1 liên kết đôi π giữa 2 nguyên tử C | Có 1 liên kết 3 (1 σ và 2 π) giữa 2 nguyên tử C | Vòng 6 cạnh, 3 liên kết đôi π xen kẽ giữa 3 liên kết σ đơn |
| Phản ứng đặc trưng | Phản ứng thế phản ứng hidro hóa | Phản ứng cộng | Phản ứng cộng | Phản ứng thế và phản ứng cộng |
| Ứng dụng chính | Làm nhiên liệu trong đời sống và sản xuất | Làm nguyên liệu sản xuất rượu etylic và axit axetic | Làm nguyên liệu trong công nghiệp và sản xuất 1 số chất hưu cơ khác | Làm dung môi và làm nguyên liệu sản xuất 1 số chất dẻo. |
• Một số phản ứng đặc trưng của Axetilen , Etilen , Benzen và Metan
CH4 + Cl2  CH3Cl + HCl
CH3Cl + HCl
C2H4 (khí) + Br2(dd) → CH2Br-CH2Br (lỏng)
C2H2 (khí) + Br2(dd) → Br2-CH-CH-Br2 (lỏng)
C6H6 (khí) + Br2(lỏng) → C6H5Br(lỏng) + HBr (khí)
Đáp án A
Do phân tử metan chỉ có liên kết đơn, còn phân tử etilen ngoài liên kết đơn, còn có liên kết đôi kém bền nên dễ tham gia phản ứng cộng