So sánh thể tích khí hidro ( đktc) thu được trong mỗi trường hợp sau:
0,1 mol Zn tác dụng với dung dịch H 2 S O 4 loãng, dư.
0,1 mol Al tác dụng với dung dịch H 2 S O 4 loãng, dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

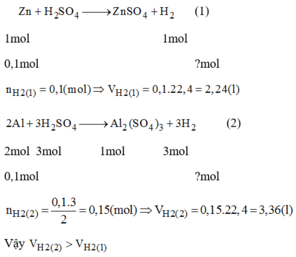

So sánh thể tích khí hiđro sinh ra
TN1 : Dùng dư axit để toàn lượng Zn tham gia phản ứng.
Theo (1) : 0,1 mol Zn điều chế được 0,1 mol H 2
Theo (2) : 0,1 mol Zn điều chế được 0,1 mol H 2
Kết luận : Những thể tích khí hiđro thu được trong thí nghiệm 1 là bằng nhau.
TN 2 - Dùng dư Zn để toàn lượng axit tham gia phản ứng.
Theo (1) : 0,1 mol HCl điều chế được 0,05 mol H 2
Theo (2) : 0,1 mol H 2 SO 4 điều chế được 0,1 mol H 2
Kết luận . Những thể tích khí hiđro thu được trong thí nghiệm 2 là không bằng nhau. Thể tích khí hiđro sinh ra ở (2) nhiều gấp 2 lần ở (1).

TH1: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,1 -----------------------------> 0,1 (mol)
=> \(V_{H_2}\)= 0,1 . 22,4 = 2,24(lít)
TH2: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO4\right)_3+3H_2\)
0,1 ------------------------------------> 0,15 (mol)
\(\Rightarrow V_{H_2}\)=0,15 . 22,4 = 3,36 (lít)
Ta thấy 2,24 < 3,36
\(\Rightarrow V_{H_2\left(TH1\right)}< V_{H_2\left(TH2\right)}\)

Đáp án A
Nhận thấy dung dịch Y có nhiều H+ hơn dung dịch X.
Gọi 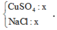
Tại thời điểm t![]()
Tại thời điểm 2t ![]() → Có OH- sinh ra ở bên catot là 0,4 mol.
→ Có OH- sinh ra ở bên catot là 0,4 mol.
![]() → x = 0,8
→ x = 0,8
![]()