
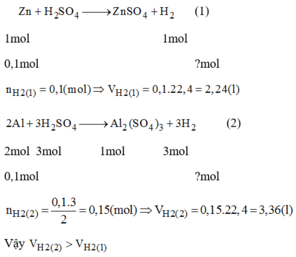
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

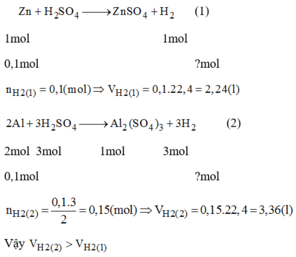

pt:2Fe+3H2SO4\(\rightarrow\)Fe2SO4+H2
a)nFe=\(\frac{m}{M}\)=\(\frac{22,4}{56}\) =0,4(mol)
nFe2(SO4)3=\(\frac{m}{M}\)=\(\frac{24,5}{340}\)=0,07(mol)
Theo pt ta có tỉ lệ :
\(\frac{0,4}{2}>\frac{0,07}{1}\)
=>nFe dư , nFe2(SO4)3
nên ta tính theo nFe2(SO4)3
=> nFe dư = nFe đề bài - nFe phản ứng
= 2-0,2=1,8(mol)
=>mFe = n x M = 1,8 x 56 = 100,8(g)
b) Theo pt: nH2 = nFe = 1,8 (mol)
VH2 = n x 22,4 = 1,8 x 22,4 = 40,32 (l)

TH1: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,1 -----------------------------> 0,1 (mol)
=> \(V_{H_2}\)= 0,1 . 22,4 = 2,24(lít)
TH2: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO4\right)_3+3H_2\)
0,1 ------------------------------------> 0,15 (mol)
\(\Rightarrow V_{H_2}\)=0,15 . 22,4 = 3,36 (lít)
Ta thấy 2,24 < 3,36
\(\Rightarrow V_{H_2\left(TH1\right)}< V_{H_2\left(TH2\right)}\)

Theo định luật BTKL ta có :
\(m_{C_2H_2}+m_{H_2}=m+m_y\)
\(\Rightarrow0,06.26+0,04.2=m+0,02.0,5.32\)
\(\Rightarrow m=1,32g\)

Gọi số mol của Cu, Fe, Al trong 23,8 gam hhX lần lượt là x, y, z mol
→ mX = 64x + 56y + 27z = 23,8 (1)
nCl2nCl2 = x + 1,5y + 1,5z = 0,65 (2)
0,25 mol X + HCl → 0,2 mol H2 nên 0,2.(x + y + z) = 0,25.(y + 1,5z) (3)
Từ (1), (2), (3) => x = 0,2 mol; y = 0,1 mol; z = 0,2 mol
%Cu=0,2.6423,8≈53,78%%Cu=0,2.6423,8≈53,78%
%Fe=0,1.5623,8≈23,53%%Fe=0,1.5623,8≈23,53%
%Al ≈ 22,69%

Gọi số mol của Cu, Fe, Al trong 23,8 gam hhX lần lượt là x, y, z mol
→ mX = 64x + 56y + 27z = 23,8 (1)
nCl2nCl2 = x + 1,5y + 1,5z = 0,65 (2)
0,25 mol X + HCl → 0,2 mol H2 nên 0,2.(x + y + z) = 0,25.(y + 1,5z) (3)
Từ (1), (2), (3) => x = 0,2 mol; y = 0,1 mol; z = 0,2 mol
%Cu=0,2.6423,8≈53,78%%Cu=0,2.6423,8≈53,78%
%Fe=0,1.5623,8≈23,53%%Fe=0,1.5623,8≈23,53%
%Al ≈ 22,69%