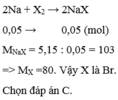Halogen hóa hoàn toàn một lượng Na nặng 1,38g bằng lượng vừa đủ halogen thấy tạo thành 3,51g muối. Tìm halogen và thể tích halogen (đktc) đã tham gia phản ứng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nAgNO3=0,2nAgNO3= 0,2 (mol)
CaX2+2AgNO3→Ca(NO3)2+2AgXCaX2+2AgNO3→Ca(NO3)2+2AgX
a, ⇒nCaX2=12.nAgNO3=0,1⇒nCaX2=12.nAgNO3=0,1(mol)
⇒CaX2=11,10,1=111⇒CaX2=11,10,1=111(mol)
⇔40+X.2=111⇔40+X.2=111
⇒X=35,5⇒X=35,5
⇒X⇒X là Cl⇒CT:CaCl2Cl⇒CT:CaCl2
b, nAgCl=2.nCaCl2=0,2nAgCl=2.nCaCl2=0,2 (mol)
⇒mAgCl=143,5.0,2=28,7(g)
a)CTHH của X: \(CaX_2\)
\(CaX_2 + 2AgNO_3 \to 2AgX + Ca(NO_3)_2\\ n_{CaX_2} = \dfrac{1}{2}n_{AgNO_3} = \dfrac{1}{2}.0,2.1 = 0,1(mol)\\ \Rightarrow M_{CaX_2} = 40 + 2X = \dfrac{11,1}{0,1} = 111\\ \Rightarrow X = 35,5(Cl)\)
Vậy muối cần tìm : \(CaCl_2\)
b)
\(n_{AgCl} = n_{AgNO_3} = 0,2(mol)\\ \Rightarrow m_{AgCl} =0,2.143,5 = 28,7(gam)\)

\(Cu+X2-->CuX2\)
\(n_{Cu}=\frac{13,44}{64}=0,21\left(mol\right)\)
\(n_{X2}=n_{Cu}=0,21\left(mol\right)\)
\(M_{X2}=\frac{33,6}{0,21}=160\)
\(=>X=80\left(Br\right)\)
Vậy......
Câu 6
\(2Na+X2-->2NaX\)
\(m_{X2}=m_{muối}-m_{Na}=9-1,38=7,62\)
\(n_{Na}=\frac{1,38}{23}=0,06\left(mol\right)\)
\(n_{X2}=\frac{1}{2}n_{Na}=0,03\left(mol\right)\)
\(M_{X2}=\frac{7,62}{0,03}=245=>X=127\left(I\right)\)

Gọi nguyên tố halogen đó là X
Các PTHH:
\(2Na+X_2-t^o\rightarrow2NaX\)
.....\(\dfrac{11,7}{2\left(23+X\right)}\)......\(\dfrac{11,7}{23+X}\).....(mol)
\(2Al+3X_2-t^o\rightarrow2AlX_3\)
....\(\dfrac{8,9.3}{2\left(27+3X\right)}\).....\(\dfrac{8,9}{27+3X}\).......(mol)
Ta có: \(\dfrac{11,7}{2\left(23+X\right)}=\dfrac{8,9.3}{2\left(27+3X\right)}\)
\(\Leftrightarrow\) X = 35,5 (Clo) \(\Rightarrow\) Halogen đó là clo

Gọi công thức chung của 2 halogen là X2
PTHH: \(3X_2+2Al\underrightarrow{t^o}2AlX_3\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\) (2)
Ta có: \(n_{HCl}=\dfrac{365\cdot1,2\cdot10\%}{36,5}=1,2\left(mol\right)\) \(\Rightarrow n_{Al\left(2\right)}=0,4\left(mol\right)\)
\(\Rightarrow n_{Al\left(1\right)}=\Sigma n_{Al}-0,4=0,6\left(mol\right)\) \(\Rightarrow n_{X_2}=0,9\left(mol\right)\)
\(\Rightarrow\overline{M}_{X_2}=\dfrac{117,3}{0,9}\approx130,3\)
Vì \(M_{Cl_2}=71< 130,3< 160=M_{Br_2}\)
\(\Rightarrow\) 2 halogen cần tìm là Clo và Brom