Khử hoàn toàn 4,06 g một oxit của kim loại R bằng khí co ở nhiệt độ cao thành kim loại . Dẫn toàn bộ khí thu được sau phản ứng vào bình đựng dung dịch \(Ca\left(OH\right)_2\) dư thấy tạo thành 7 g kết tủa trắng .Nếu lấy lượng kim loại sinh ra hòa tan hết vào dd HCl dư thì thu được 1,176 lít khí \(H_2\) (đktc). Xác định CT oxit của kim loại R.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CT của oxit cần tìm là RxOy
RxOy+yCO→xR+yCO2 (1)
CO2+Ca(OH)2→CaCO3+H2O (2)
Vì Ca(OH)2 dư nên nCO2=n↓=0,07 mol
Theo PTHH (1), nO trong oxit=nCO2=0,07 mol
→mO trong oxit=0,07.16=1,12 g
→mR trong oxit=4,06−1,12=2,94 g
+) Cho kim loại R tác dụng với dung dịch HCl
PTHH: 2R+2nHCl→2RCln+nH2 (3)
Ta có: nH2=0,0525 mol
Theo (3), nR=\(\dfrac{2}{n}\)H2=\(\dfrac{0,105}{n}\)
→\(\dfrac{0,105}{n}R\)=2,94→R=28n
Chỉ có cặp nghiệm duy nhất thỏa mãn:
\(\left\{{}\begin{matrix}n=2\\R=56\left(Fe\right)\end{matrix}\right.\)
→nFe=0,0525 mol
Khi đó ta có: \(\dfrac{x}{y}:\dfrac{nFe}{nO}:\dfrac{0,0525}{0,07}=\dfrac{3}{4}\)
Vậy CT của oxit kim loại cần tìm là: Fe3O4

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
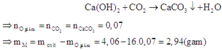
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
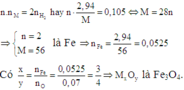
Đáp án D.

`a)`
Oxit: `Fe_xO_y`
`Fe_xO_y+yCO` $\xrightarrow{t^o}$ `xFe+yCO_2`
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
Theo PT: `n_{CO_2}=n_{CaCO_3}=7/{100}=0,07(mol)`
`->n_{Fe_xO_y}={n_{CO_2}}/y={0,07}/y(mol)`
`->M_{Fe_xO_y}={4,06}/{{0,07}/y}=58y`
`->56x+16y=58y`
`->x/y={42}/{56}=3/4`
`->` Oxit: `Fe_3O_4`
`b)`
`n_{Fe_3O_4}={4,06}/{232}=0,0175(mol)`
`2Fe_3O_4+10H_2SO_4->3Fe_2(SO_4)_3+SO_2+10H_2O`
Đề thiếu.

Đáp án C
nCO2 = nCaCO3 = 0,07 mol
O + CO → CO2
0,07 ← 0,07
mKL = moxit – mO
= 4,06 – 0,07.16 = 2,94 (g)
Gọi hóa trị của KL khi tác dụng với HCl là n
M → 0,5n H2
0,105/n← 0,0525 (mol)
![]()
![]()
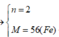
![]()
![]()

M2On+nCO->nCO2+2M
2M+2nHCl->2MCln+nH2
nCO2=14/100=0,14(mol)
=>mM=8,12-0,14x16=5,88(g)
nH2=2,352/22,4=0,105(mol)
=>nM=0,21/n(mol)
M=5,88:0,21/n=28n
n=2 M=56=>M là Fe
Ta có nFe:nO=0,105:0,14=3: 4
=>CTHH oxit là Fe3O4
Khí sinh ra là CO2.
Có: \(n_{CaCO_3}=\dfrac{14}{100}=0,14\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
___0,14_______________0,14 (mol)
Bản chất của khử oxit kim loại: \(CO+O_{\left(trongoxit\right)}\rightarrow CO_2\)
⇒ nO (trong oxit) = 0,14 (mol)
Mà: m oxit = mKL + mO (trong oxit)
⇒ mKL = 8,12 - 0,14.16 = 5,88 (g)
Giả sử KL đó là A, có hóa trị n.
Ta có: \(n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
PT: \(2A+2nHCl\rightarrow2ACl_n+nH_2\)
Theo PT: \(n_A=\dfrac{2}{n}n_{H_2}=\dfrac{0,21}{n}\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{5,88}{\dfrac{0,21}{n}}=28n\left(g/mol\right)\)
Với n = 2, MA = 56 (g/mol) là thỏa mãn.
⇒ A là Fe và \(n_{Fe}=\dfrac{5,88}{56}=0,105\left(mol\right)\)
Giả sử oxit cần tìm có công thức là FexOy.
\(\Rightarrow x:y=0,105:0,14=3:4\)
Vậy: Oxit cần tìm là Fe3O4 (Oxit sắt từ)
Bạn tham khảo nhé!

\(n_{CO} = n_{CO_2} = n_{BaCO_3} = \dfrac{94,56}{197} = 0,48(mol)\)
Bảo toàn khối lượng :
\(m_{kim\ loại} = m_{oxit} + m_{CO} - m_{CO_2} = 27,84 + 0,48.28 -0,48.44 = 20,16(gam)\)
\(n_{H_2} = \dfrac{8,064}{22,4} = 0,36(mol)\)
2R + 2nHCl → 2RCln + nH2
\(\dfrac{0,72}{n}\).............................0,36...........(mol)
Suy ra: \(\dfrac{0,72}{n}\).R = 20,16 ⇒ R = 28n. Với n = 2 thì R = 56(Fe)
CO + Ooxit → CO2
0,48.....0,48...............(mol)
Ta có: \(\dfrac{n_{Fe}}{n_O} = \dfrac{0,36}{0,48} = \dfrac{3}{4}\). Vậy oxit sắt là Fe3O4

\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Gọi CTHH của oxit là XaOb
PTHH: XaOb + bCO --to--> aX + bCO2
\(\dfrac{0,2}{b}\)<---------------\(\dfrac{0,2a}{b}\)<-0,2
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,2<------0,2
=> \(M_{X_aO_b}=a.M_X+16b=\dfrac{16,2}{\dfrac{0,2}{b}}=81b\left(g/mol\right)\)
=> \(\dfrac{a}{b}=\dfrac{65}{M_X}\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2X + 2nHCl --> 2XCln + nH2
\(\dfrac{0,4}{n}\)<---------------------0,2
=> \(\dfrac{0,2a}{b}=\dfrac{0,4}{n}\)
=> \(\dfrac{13}{M_X}=\dfrac{0,4}{n}\) => \(M_X=\dfrac{65}{2}n\left(g/mol\right)\)
- Nếu n = 1 => Loại
- Nếu n = 2 => MX = 65 (g/mol)
=> X là Zn
\(\dfrac{x}{y}=1\) => CTHH: ZnO
- Nếu X = 3 => Loại
Vậy CTHH của oxit là ZnO
Gọi oxit kim loại là MxOy.
MxOy + yCO → xM + yCO2
nCaCO3 = 0,2 mol → nCO2 = 0,2 mol
Số mol của oxi có trong oxit = số mol CO = số mol CO2 = 0,2 mol
→ khối lượng của oxi có trong oxit là 0,2.16 = 3,2 gam
mO + mM = 16,2 gam → mM = 13 gam
2M + 2nHCl → 2MCln + nH2
0,2.2/n ← 0,2 mol
mM = 13 gam, nM = 0,4/n mol
→ M = 13.n/0,4 = 32,5n
Xét n = 1 → M = 32,5 (loại)
n = 2 → M = 65 → M là Zn
nZn : nO = 1 : 1 → Công thức của oxit là ZnO

BL
CO2+Ca(OH)2==>CaCO3+H20
0.07<= 0.07
đây là bài toán lừa đó bạn ạ . hóa trị của KL thay đổi nên gọi n m lan luot la hoa trị trong oxit và trong KL
ta gọi KL la M
M+ nHCL= MCLm+ (n/2) H2
1.76/22.4
từ PT khử thành KL áp dụng định luật BTKL ta có
mM=4.06+0.07*28-0.07*44=2.94 g
==> M=18.7n
xét từng trường hợp => M=56==> Fe . CT oxit Fe3O4
Chúc bn học tốt![]()
- Khi dẫn CO2 vào Ca(OH)2 dư thì nCO2 \(=n_{CaCO3}=\frac{7}{100}=0,07\left(mol\right)\)
- Quá trình khử oxit hiểu đơn giản là:
\(C+O_2\rightarrow CO_2\)
\(\Rightarrow n_{O\left(oxit\right)}=n_{CO2}=0,07\left(mol\right)\)
\(\Rightarrow m_{kl}=m_{oxit}-m_O=4,06-0,07.16=2,94\left(g\right)\)
- Khi cho KL tác dụng với HCl:
\(2X+2nHCl\rightarrow2XCl_n+nH_2\)
0,105/n_______________0,0525 _(mol)
Ta có :
\(m_X=\frac{0,105}{n}.M_X=2,94\Rightarrow M_X=28n\)
Thay n = 1, 2, 3 vào thấy với n = 2; MX = 56 thỏa mãn → KL là Fe
\(\Rightarrow n_{Fe}:n_O=0,0525:0,07=3:4\)
Vậy CT oxit là Fe3O4