Bài 5: Hãy tự chọn một thuốc thử để nhận biết 3 dd mất nhãn: Na2CO3, Na2SO4 và Ba(NO)2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cho các chất tác dụng lần lượt với nhau ta được bảng sau :
| Ba(HCO3)2 | Na2CO3 | NaHCO3 | Na2SO4 | NaHSO4 | |
| Ba(HCO3)2 | - | tủa | - | tủa | tủa+khí |
| Na2CO3 | tủa | - | - | - | khí |
| NaHCO3 | - | - | - | - | khí |
| Na2SO4 | tủa | - | - | - | - |
| NaHSO4 | tủa+khí | khí | khí | - | - |
Dung dịch nào tạo 2 kết tủa, 1 vừa kết tủa, vừa tạo khí => Ba(HCO3)2
Dung dịch nào tạo 1 kết tủa, 1 khí thoát ra => Na2CO3
Dung dịch nào tạo 1 khí thoát ra => NaHCO3
Dung dịch nào tạo 1 kết tủa => Na2SO4
Dung dịch nào tạo 2 khí thoát ra, 1 vừa kết tủa, vừa tạo khí => NaHSO4

Làm xong chắc vứt não ra ngoài luôn á
Để nhận biết được NaCl, AgNO3 và Na2CO3, ta có thể sử dụng thuốc thử Ba(NO3)2. Khi Ba(NO3)2 tác dụng với NaCl, AgNO3 và Na2CO3, ta thu được các kết tủa khác nhau:
+ Khi Ba(NO3)2 tác dụng với NaCl, ta thu được kết tủa trắng là BaCl2.
+ Khi Ba(NO3)2 tác dụng với AgNO3, ta thu được kết tủa trắng là Ba(NO3)2.
+ Khi Ba(NO3)2 tác dụng với Na2CO3, ta thu được kết tủa trắng là BaCO3.
Vậy, ta có thể sử dụng Ba(NO3)2 để nhận biết được cả 3 chất NaCl, AgNO3 và Na2CO3.
Bạn ơi cho mỉm hỏi là cả ba đều nhận đc kết tủa trắng thì sao mà nhận biết đc ạ

b) Cho quỳ tím ẩm vào từng mẫu thử
+ Hóa đỏ quỳ : SO2, CO2
+ Không hiện tượng : H2, N2
Dẫn 2 mẫu thử làm quỳ hóa đỏ qua dung dịch Brom
+ Mất màu dung dịch Brom : SO2
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
+ Không hiện tượng : CO2
Dẫn 2 mẫu thử làm quỳ không đổi màu qua bột CuO màu đen, nung nóng
+ Có chất rắn màu đỏ xuất hiện : H2
\(H_2+CuO-^{t^o}\rightarrow Cu+H_2O\)
+ Không hiện tượng : N2
c) Cho các mẫu thử vào nước
+ Tan, có khí thoát ra : Ca
+ Tan : CaO, P2O5
+ Không tan : Mg, MgO
Cho quỳ tím vào dung dịch của 2 mẫu thử tan trong nước
+ Quỳ hóa xanh : CaO
+ Quỳ hóa đỏ : P2O5
Lấy dung dịch tan trong nước của P2O5 cho tác dụng với 2 mẫu thử không tan trong nước
+ Xuất hiện kết tủa, có khí thoát ra : Mg
3Mg + 2H3PO4 → Mg3(PO4)2 + 3H2
+ Xuất hiện kết tủa : MgO
3MgO + 2H3PO4 → Mg3(PO4)2 + 3H2O

Đáp án D
Lấy BaCl2 cho lần lượt vào 3 mẫu thử.
Các phương trình phản ứng xảy ra:
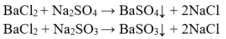
Mẫu không có kết tủa là HCl. Lấy HCl cho vào kết tủa, BaSO3 tan.
![]()

* Dung dịch kiềm
( ví dụ NaOH… ) * Kết tủa xanh lơ : Cu(OH)2
Muối của Fe(II)
(dd lục nhạt ) * Kết tủa trắng xanh bị hoá nâu đỏ trong nước :
2Fe(OH)2 + H2O + ½ O2 2Fe(OH)3
( Trắng xanh) ( nâu đỏ )
Muối Fe(III) (dd vàng nâu) * Kết tủa nâu đỏ Fe(OH)3
d.dịch muối Al, Cr (III) …
( muối của Kl lưỡng tính ) * Dung dịch kiềm, dư * Kết tủa keo tan được trong kiềm dư :
Al(OH)3 ( trắng , Cr(OH)3 (xanh xám)
Al(OH)3 + NaOH NaAlO2 + 2H2O

Lấy mỗi chất ra một ít và làm thí nghiệm sau:
- Cho từng mẫu thử nhỏ giọt vào dung dịch phenol:
+ mẫu làm phenol chuyển hồng là \(Ba\left(OH\right)_2\)
+ mẫu làm phenol mất màu là `HCl`
+ không hiên tượng: \(BaCl_2,Na_2SO_4,NaNO_3\) (I)
- Cho dung dịch \(Ba\left(OH\right)_2\) vừa nhận biết được tác dung dư với các chất chưa phân biệt được ở nhóm (I):
+ có hiện tượng kết tủa trắng là `Na_2SO_4`
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
+ không hiện tượng: \(BaCl_2,NaNO_3\) (II)
- Cho dung dịch `Na_2SO_4` tác dụng dư vớ các chất ở nhóm (II):
+ có hiện tượng kết tủa trắng là `BaCl_2`
\(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4\)
+ không hiện tượng là `NaNO_3`
- Đổ dd H2SO4 vào các dd
+) Xuất hiện khí: Na2CO3
PTHH: \(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+CO_2\uparrow\)
+) Xuất hiện kết tủa: Ba(NO3)2
PTHH: \(Ba\left(NO_3\right)_2+H_2SO_4\rightarrow2HNO_3+BaSO_4\downarrow\)
+) Không hiện tượng: Na2SO4