1. một hỗn hợp gồm Fe2O3 va MgO nang 16g duoc hoa tan het trong dd axit HCl , sau đó đem cô cạn dd thu được 35,25 g muối khan
a.viết các PTHH
b, Tính thành phần % klg mỗi oxit trong hỗn hợp đầu.
2.cho 42,8 hỗn hợp A gồm đồngng (II)oxit và kali oxit vào nước (dư)khuấy đều, sau phản ứng thu được160ml dd B 2,5 M va a g chất rắn C
a. tính giá trị của a?
b. để hoà tan hết C trên cần mấy ml dd HCl 7,3% (D=1,15g/ml)
giúp mình giải đầy đủ nha


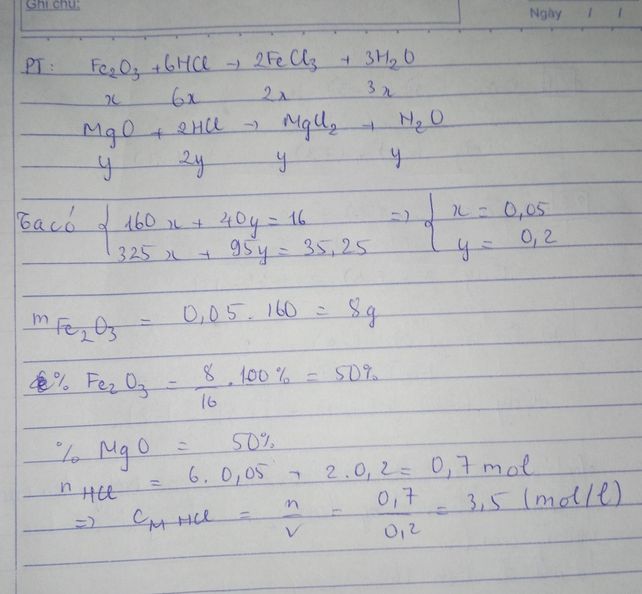

bài1
Gọi x và y là số mol của \(Fe_2O_3\) và MgO (x,y>0)
Có \(160x+40y=16\left(1\right)\)
PTHH \(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
x 2x (mol)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
y y (mol)
Lại có \(325x+95y=35,25\left(2\right)\)
Từ (1) và (2) ta có hpt
\(\left\{{}\begin{matrix}160x+40y=16\\325x+95y=35,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Fe_2O_3}=0,05\times160=8\left(g\right)\Leftrightarrow\%Fe_2O_3=\frac{8}{16}100\%=50\%\)\(\Rightarrow\%MgO=100\%-50\%=50\%\)
Bài 2
\(K_2O+H_2O\rightarrow2KOH\)
\(n_{KOH}=0,16\times2,5=0,4\left(mol\right)\rightarrow m_{KOH}=0,4\times56=22,4\left(g\right)\)\(\Rightarrow a=m_{CuO}=42,8-22,4=20,4\left(g\right)\)
b) \(n_{CuO}=\frac{20,4}{80}=0,255\left(mol\right)\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
Theo PTHH \(n_{HCl}=2n_{CuO}=0,51\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,51\times36,5=18,615\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\frac{18,615\times100}{7,3}=255\left(g\right)\)
Lại có \(D=\frac{m}{V}\Rightarrow V_{HCl}=\frac{255}{1,15}\approx221,74\left(ml\right)\)