Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ở phần b, nếu trong hỗn hợp đầu thì phải là % khối lượng mỗi oxit chứ nhỉ? Và ở phần c phải là 1,1 g/ml chứ không phải g/mol bạn nhé!


Bạn tham khảo link nhé!
một hỗn hợp gồm Fe2O3 và MgO nặng 16g được hòa tan hết trong udng dịch axit HCL sau đó đem cô cạn dung dịch thu được 35,25g muối khan a) viết các PTHH b) tính thành phần % khối lượng mỗi oxit trong hỗn hợp ban đầu >< giúp với ạ - Hoc24

Bài 2 :
PTHH :
CaO + 2HCl ----> CaCl2 + H2 (PT1)
CaCO3 + 2HCl ------> CaCl2 + CO2 + H2O (PT2)
Phản ứng hoàn toàn :
Ta có : nCO2 = 4,48 : 22,4 = 0,2 (mol)
=> nCaCO3 = 0,2 (mol) => nCaCl2 (PT2) = 0,2 (mol)
=> mCaCO3 = 0,2 . (40 + 12 + 48) = 20 (g)
Ta thấy : dd B có chứa CaCl2 của PT1 và PT2
Sau khi cô cạn dung dịch B thì dd còn lại muối CaCl2
Ta có : mCaCl2 (PT2) = 0,2 . (40 + 71) =22,2 (g)
=> 22,2 + mCaCl2 (PT1) = 66,6
=> mCaCl2 (PT1) = 44,4 (g)
=> nCaCl2 (PT1) = 44,4 : (40 + 71) = 0,4 (mol)
=> nCaO = 0,4 (mol)
=> mCaO = 0,4 . (40 + 16) = 22,4 (g)
b)
nHCl (cần dùng) = nHCl (PT1) + nHCl (PT2) = 0,8 + 0,4 = 1,2 (mol)
=> mHCl (cần dùng) = 1,2 . 36,5 = 43,8 (g)
=> mdd HCl 7,3% = 43,8 : 7,3% = 600(g)
Bài 1 :
Ta có PTHH :
(1) \(Mg+2HCl->MgCl2+H2\uparrow\)
(2) \(MgCO3+2HCl->MgCl2+H2O+CO2\uparrow\)
Vì khí H2 không làm đục nước vôi trong Ca(OH)2 nên nó sẽ không phản ứng
=> khí không màu sau p/ư là H2 => VH2 = 2,8(l) => nH2 = \(\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
=> nMg = 0,125 mol
Ta có : mkt = mCaCO3 = 10(g) => nCaCO3 = 0,1(mol)
Ta có PTHH 3 :
\(CO2+Ca\left(OH\right)2->CaCO3+H2O\)
0,1mol................................0,1mol
=> nCO2 = 0,1(mol)
=> nMgCO3 = 0,1 (mol)
a) Ta có :
%mMg = \(\dfrac{0,125.24}{0,125.24+0,1.84}.100\%\approx26,32\%\)
%mMgCO3 = 100% - 26,32% = 73,68%
b) Ta có : nHCl(1) = 2nH2 = 0,25 mol ; nCO2(2) = 2nCo2 = 0,2 mol
VddHCl = \(\dfrac{0,25+0,2}{0,5}=0,9\left(M\right)\)
Ta có : nMgCl2(1) = nH2 = 0,125 mol ; nMgCl2(2) = nCo2 = 0,1(mol)
Ta có : \(CM_{MgCl2}=\dfrac{0,125+0,1}{0,9}=0,25\left(M\right)\)
Bài 2 :
Theo đề bài ta có : nCo2 = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Ta có PTHH :
(1) \(CaO+2HCl->CaCl2+H2O\)
(2) \(CaCO3+2HCl->CaCl2+H2O+CO2\uparrow\)
0,2mol..........0,4mol..........0,2mol................0,2mol
DD B thu được là CaCl2
a) Ta có :
mCaCl2(2) = 0,2.111 = 22,2(g)
=> mCaCl2(1) = 66,6 - 22,2 = 44,4(g)
Theo PTHH 1 ta có : nCaO = nCaCl2 = \(\dfrac{44,4}{111}=0,4\left(mol\right)\)
=> Khối lượng mỗi chất trong A là :
mCaO = 0,4.56 = 22,4(g)
mCaCO3 = 0,2.100 = 20(g)
b) ta có : nHCl(1) = 2nCaO = 2.0,4 = 0,8(mol)
=> nHCl = nHCl(1) + nHCl(2) = 0,8 + 0,2 = 1 mol
=> mddHCl = \(\dfrac{1.36,5}{7,3}.100=500\left(g\right)\)
Vậy..............

Bai 1
Ta co pthh
2Al + 6HCl \(\rightarrow\)2AlCl3 + 3H2
Mg + 2HCl \(\rightarrow\)MgCl2 + H2
a,Theo de bai ta co
Khoi luong cua moi chat trong 1 mol hon hop la
mAl=\(\dfrac{36.7,5}{100}=2,7g\)
mMg = 7,5 - 2,7 =4,8 g
So mol cua moi chat la
nAl=\(\dfrac{2,7}{27}=0,1mol\)
nMg=\(\dfrac{4,8}{24}=0,2mol\)
b,Theo 2 pthh ta co
nH2=\(\dfrac{3}{2}nAl=\dfrac{3}{2}.0,1=0,15mol\)
nH2=nMg=0,2 mol
\(\Rightarrow\)VH2=(0,15 + 0,2 ) .22,4=7,84 l
Bai 2 ta co pthh
CuO + H2 \(\rightarrow\)Cu + H2O
Fe2O3 + 3H2\(\rightarrow\)2Fe + 3H2O
Theo de bai ta co
nH2 =\(\dfrac{25,76}{22,4}=1,15mol\)
Goi x mol la so mol cua H2 tham gia vao pthh1
So mol cua H2 tham gia vao pthh 2 la 1,15-x mol
Theo pthh
nCuO =nH2=x mol
nFe2O3=\(\dfrac{1}{3}nH2=\dfrac{1}{3}.\left(1,15-x\right)mol\)
Theo de bai ta co he pt
80x + 160.\(\dfrac{1}{3}\left(1,15-x\right)\)=68
\(\Leftrightarrow\)80x + 61,3 -53,3x =68
\(\Leftrightarrow\)26,7x =6,7
\(\Rightarrow\)x=0,3 mol
\(\Rightarrow\)nFe2O3 =\(\dfrac{1}{3}nH2=\dfrac{1}{3}.0,3=0,1mol\)
nCuO=nH2 =0,3 mol
\(\Rightarrow\)thanh phan % khoi luong la
%mCuO =\(\dfrac{\left(0,3.80\right).100}{68}\approx35,3\%\)
%mFe2O3= 100 -35,3=64,7 %

Câu 2;
Đặt CT của muối cacbonat kim loại là \(M_2\left(CO3\right)_x\)
\(n_{Ca\left(OH\right)2}=\dfrac{150.1}{1000}=0,15mol\)
\(n_{CaCO3}=10:100=0,1mol\)
PT: (1) \(M_2\left(CO3\right)_x+2xHCl->2MCl_x+xH_2O+xCO_{ }_2\)
KHí A là CO2 và H2O. Cho tác dụng với \(Ca\left(OH\right)_2\) thì chỉ có CO2 phản ứng, ta có pt:
PT (2) \(CO_2+Ca\left(OH\right)_2->CaCO3+CO2+H2O\)
0,15 0,1
=> n Ca(OH)2 dư 0,05 mol
-> nCO2(pt2)= 0,1 mol
PT (3) : 2CO2+ Ca(OH)2 -> 2Ca(H2CO3)2
0,05
-> nCO2(pt3) = 0,05.2=0,1 mol
=> tổng nCO2= 0,1+0,1=0,2 mol
Theo pt1 => \(n_{M2\left(CO3\right)x}\)= \(\dfrac{0,2}{x}\)mol
=> m M2(CO3)x= (2M+60x).\(\dfrac{0,2}{x}\)=\(\dfrac{0,4}{x}\)+12=16,8g
<=> \(\dfrac{M}{x}\)=12
xét bảng ta đượ x=2 và m=24
=> M là Magie => CTHH: MgCO3.
Có đúng không?

Hòa tan 10,2g hỗn hợp chứa Mg và Al vào dd axit HCl vừa đủ. Sau phản ứng thu được 11,2 lít khí H2 (đktc)
a) Tính % khối lượng mỗi chất trong hỗn hợp ban đầu
b) Tính khối lượng dd HCl 7,3% cần dùng
c) Tính khối lượng hh muối thu được sau khi cô cạn dung dịch sau phản ứng
d) Tính nồng độ % các chất có trong dd sau phản ứng
a) 10,2 gam hỗn hợp gồm: \(\left\{{}\begin{matrix}Mg:a\left(mol\right)\\Al:b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow24a+27b=10,2\left(I\right)\)
\(n_{H_2}\left(đktc\right)=0,5\left(mol\right)\)
\(Mg\left(a\right)+2HCl\left(2a\right)\rightarrow MgCl_2\left(a\right)+H_2\left(a\right)\)
\(2Al\left(b\right)+6HCl\left(3b\right)\rightarrow2AlCl_3\left(b\right)+3H_2\left(1,5b\right)\)
Theo PTHH: \(\sum n_{H_2}=a+1,5b\left(mol\right)\)
\(\Rightarrow a+1,5b=0,5\left(II\right)\)
Giair (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
=> Phần trăm khối lương
b) Theo PTHH: \(\sum n_{HCl}=1\left(mol\right)\Rightarrow m_{HCl}=36,5\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{36,5.100}{7,3}=500\left(g\right)\)
c) Muối sau phản ứng\(\left\{{}\begin{matrix}MgCl_2:0,2\left(mol\right)\\AlCl_3:0,2\left(mol\right)\end{matrix}\right.\)
=> Khối lượng hôn hợp muối thu được khi cô cạn dung dịch sau pứ
d) \(m_{ddsau}=m_{hh}+m_{ddHCl}-m_{H_2}\\ =10,2+500-1=509,2\left(g\right)\)
=> nồng độ % các chất có trong dd sau phản ứng

Bài 1 :
Phản ứng xảy ra:
\(Fe_2O_3+6HNO_3\rightarrow2Fe\left(NO_3\right)_3+3H_2O\)
\(CuO+2HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\)
Ta có :
\(n_{HNO3}=\frac{18,9}{63}=0,3\left(mol\right)\)
Bảo toàn nguyên tố H: \(n_{H2O}=\frac{1}{2}n_{HNO3}=0,15\left(mol\right)\)
BTKL,
\(m_{oxit}+m_{HNO3}=m_{muoi}+m_{H2O}\)
\(\Leftrightarrow20+18,9=a+0,15.18\)
\(\Rightarrow a=36,2\left(g\right)\)
Gọi số mol Mg và Al trong phần 1 lần lượt là a, b.
Cho phần 1 tác dụng với oxi.
\(2Mg+O_2\rightarrow2MgO\)
\(4Al+3O_2\rightarrow2Al_2O_3\)
Ta có:
\(n_{O2}=\frac{4,48}{22,4}=0,2\left(mol\right)=\frac{1}{2}n_{Mg}+\frac{3}{4}n_{Al}=0,5a+0,75b\)
\(n_{MgO}=n_{Mg}=a\left(mol\right)\)
\(n_{Al2O3}=\frac{1}{2}n_{Al}=0,5b\left(mol\right)\)
\(\Rightarrow40a+102.0,5b=14,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
Giả sử phần 2 gấp k lần phần 1, chứa 0,1k mol Mg và 0,2k mol Al.
Cho phần 2 tác dụng với HCl
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(n_{H2}=n_{Mg}+\frac{3}{2}n_{Al}=0,1k+\frac{3}{2}.0,2k=0,4k=\frac{13,44}{22,4}=0,6\)
\(\Rightarrow k=1,5\)
Vậy ban đầu A chứa 0,25 mol Mg và 0,5 mol Al.
\(x=0,25.24+0,5.27=19,5\left(g\right)\)
\(m_{Mg}=0,25.24=6\left(g\right)\)
\(\Rightarrow\%m_{Mg}=\frac{6}{19,5}=30,77\%\)
\(\Rightarrow\%m_{Al}=100\%-30,77\%=69,23\%\)
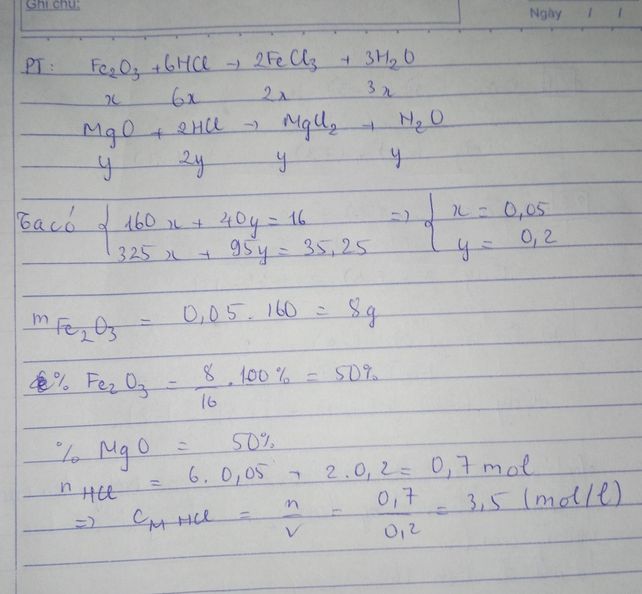
mCa(OH)2 = 7.4 g
nCa(OH)2 = 0.1 mol
Ca(OH)2 + 2HCl --> CaCl2 + 2H2O
0.1________________0.1
mCaCl2 = 0.1*111 = 11.1 g
=> mM còn lại = 46.35 - 11.1 = 35.25 g
Đặt :
nFe2O3 = x mol
nMgO = y mol
<=> 160x + 40y = 16 (1)
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
x_________________2x
MgO + 2HCl --> MgCl2 + H2O
y_______________y
<=> 325x + 95y = 35.25 (2)
(1) và (2) :
x =0.05
y = 0.2
mFe2O3 = 8 g
mMgO = 8 g
%Fe2O3 = %MgO = 8/16*100% = 50%
PTHH: Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O
Mol: x 6x 2x 3x
MgO + 2HCl ---> MgCl2 + H2O
Mol: y 2y y y
2HCl + Ca(OH)2 ---> H2O + CaCl2
Mol: 0,2 0,1 0,1 0,1
mCa(OH)2 = 14,8%*50 / 100% = 7,4g
nCa(OH)2 = 7,4 / 74 = 0,1 mol
Gọi x, y là số mol của Fe2O3, MgO
mhh = 160x + 40y = 16 (1)
mmuối = 162,5 * 2x + 95y = 35,25 (2)
Giải pt (1), (2) ==> x = 0,05 y = 0,2
%mFe2O3 = 160*0,05*100%/ 16 = 50%
%mMgO = 100% - 50% = 50%