cho 8.7 g MnO2 tác dụng với axit HCl dư, sau phản ứng thu được 1.9l khí clo (đkc). hiệu suất của phản ứng là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\ PTHH:MnO_2+4HCl_{đặc,nóng}\rightarrow MnCl_2+Cl_2+2H_2O\\ n_{Cl_2\left(TT\right)}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\\ n_{Cl_2\left(LT\right)}=n_{MnO_2}=0,2\left(mol\right)\\ \Rightarrow H=\dfrac{n_{Cl_2\left(TT\right)}}{n_{Cl_2\left(LT\right)}}.100\%=\dfrac{0,16}{0,2}.100=80\%\)

\(m_{MnO_2\left(pư\right)}=\dfrac{43,5.85}{100}=36,975\left(g\right)\)
=> \(n_{MnO_2\left(pư\right)}=\dfrac{36,975}{87}=0,425\left(mol\right)\)
PTHH: MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,425-------------------->0,425
=> VCl2 = 0,425.22,4 = 9,52 (l)
MnO2 (0,5 mol) + 4HCl \(\xrightarrow[H=85\%]{t^o}\) MnCl2 + Cl2 (0,425 mol) + 2H2O.
Thể tích khí clo thu được (đktc) là 0,425.22,4=9,52 (lít).

\(4HCl+MnO2-->Cl2+2H2O+MnCl2\)
\(n_{MnO2}=\frac{17,4}{87}=0,2\left(mol\right)\)
\(n_{Cl2}=n_{MnO2}=0,2\left(mol\right)\)
\(V_{Cl2}=0,2.22,4=4,48\left(l\right)\)
\(H\%=\frac{3,8}{4,48}.100\%=84,82\%\)

\(n_{C_6H_5Cl}=\dfrac{78}{112,5}=\dfrac{52}{75}\left(mol\right)\)
\(n_{C_6H_6}=\dfrac{78}{78}=1\left(mol\right)\)
PTHH:
\(C_6H_6+Cl_2\xrightarrow[t^o]{Fe}C_6H_5Cl\)
1------------------>1
\(\Rightarrow H=\dfrac{\dfrac{52}{75}}{1}.100\%=69,33\%\)

Câu 1 :
$n_C = \dfrac{4,8}{12} = 0,4(mol) ; n_{O_2} = \dfrac{7,437}{24,79} = 0,3(mol)$$
$C + O_2 \xrightarrow{t^o} CO_2$
Ta thấy :
$n_C : 1 > n_{O_2} : 1$ nên C dư
$n_{C\ pư} = n_{O_2} = 0,3(mol) \Rightarrow m_{C\ dư} = (0,4 - 0,3).12 = 1,2(gam)$
$\Rightarorw V_{CO_2} = V_{O_2} = 7,437(lít)$
Câu 2 :
$n_{Mg} = \dfrac{2,4}{24} = 0,1(mol)$
$n_{Cl_2} = \dfrac{9,916}{24,79} = 0,4(mol)$
$Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
Ta thấy :
$n_{Mg} : 1 < n_{Cl_2} : 1$ nên $Cl_2$ dư
$n_{Cl_2\ pư} = n_{Mg} = 0,1(mol) \Rightarrow m_{Cl_2\ dư} = (0,4 - 0,1).71 = 21,3(gam)$
$n_{MgCl_2}= n_{Mg} = 0,1(mol) \Rightarrow m_{MgCl_2} = 0,1.95 = 9,5(gam)$

nH2 = \(\dfrac{11,1555}{24,79}=0,45\left(mol\right)\)
PTHH: 2M + 2xHCl -> 2MClx + xH2
0,9 <-------------- 0,45
mHCl = 0,9 . 36,5 = 32,85 (g)
mH2 = 0,45 . 2 = 0,9 (g)
Áp dụng ĐLBTKL, ta có:
mM + mHCl = mMClx + mH2
=> mM = 40,04 + 0,9 - 32,85 = 8,09 (g)
%mM = \(\dfrac{8,09}{10}=80,9\%\)

Đáp án C
![]()
MnO2 + 4HCl →MnCl2 + 2H2O + Cl2
0,1 →0,1 (mol)
Do H% = 85% => ![]() = 0,085 (mol)
= 0,085 (mol)
V = 0,085.22,4 = 1,904 (lít)

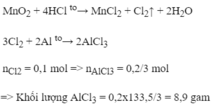

nMnO2= 8,7/87 = 0,1 (mol)
MnO2+4HCl-->MnCl2+2H2O+Cl2
0,1 . ----->0,1
VCl2(lí thuyết)= 0,1 x 22,4= 2,24 (l)
H%Cl2= 1,9/2,24 x100% \(\approx\)85%
Nếu đúng thì cho mik 1 like nha
Nếu bạn xài điện thoại thì phóng to bài viết chỗ công cụ sẽ thấy rõ hơn