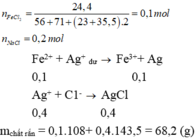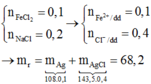Hào tan 24,9 gam hỗn hợp gồm FeCl2 và NaCl (tỉ lệ số mol tương ứng là 3: 2) vào một lượng nước dư thu được dung dịch X .Cho dd AgNO3 dư vào ddX sau pư xảy ra hoàn toàn sinh ra m gam chất rắn .Giá trị m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án A
nFeCl2 = 0,1 mol; nNaCl = 0,2 mol
Chất rắn gồm Ag và AgCl
⇒ mCR = 0,1 . 108 + 143,5 . (0,1. 2 + 0,2) = 68,2g

Gọi số mol của FeCl2 là x
→ 127x + 58,5.2.x= 24,4 => x = 0,1.
FeCl2 + 2AgNO3 --> 2AgCl + Fe(NO3)2
0,1------>0,2--------> 0,2-------> 0,1 mol
NaCl + AgNO3 ---> AgCl + NaNO3
0,2-------> 0,2------> 0,2
Fe(NO3)2 + AgNO3 --> Fe(NO3)3 + Ag
0,1---------------------------------> 0,1
m = (0,2 + 0,2)143,5 + 108.0,1 = 68,2 (g)
=> Đáp án A

Đáp án : A
Ta có : n F e C l 2 = 0,1 ; nNaCl = 0,2 mol
Fe2+ + Ag+-> Fe3+ + Ag
Ag+ + Cl--> AgCl
=> m = mAgCl + mAg = 68,2g

Từ tỉ lệ và khối lượng ban đầu tính được số mol FeCl2 = 0,02 và số mol NaCl = 0,04.
FeCl2 + 2AgNO3 ® 2AgCl + Fe(NO3)2
0,02 ® 0,04 ® 0,02
NaCl + AgNO3 ® AgCl + NaNO3
0,04 ® 0,04
Fe(NO3)2 + AgNO3 ® Fe(NO3)3 + Ag
0,02 ® 0,02.
Khối lượng chất rắn: m = 11,5 gam.
Đáp án C.