Câu1: Dung dịch tác dụng được với dung dịch Ba(OH)2 là?
A. KCl B.KNO3
C. K2SO4 D. NaCl
Câu2: Nung 5,8gam bazơ của một kim loại M có hoá trị 2 đến khối lượng không đổi thu được 4gam chất rắn.M là kim loại nào?
Câu3: Hợp chất của phi kim X với oxi có công thức hoá học là XO2 trong đó nguyên tố X chiếm 50% theo khối lượng. X là nguyên tố?
Câu4: Chất tác dụng được với dung dịch FeCl3 là:
A. KOH B.Mg(OH)2
C. Zn(OH)2 D. CuO
Câu5: Trộn 100ml dung dịch Mg(NO)3 1M với dung dịch Ba(OH)2 1,5M. Khối lượng kết tủa thu được là?
KHUÊVŨ

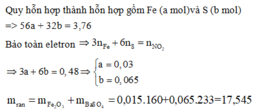



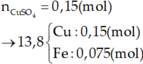
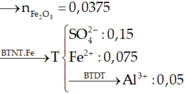
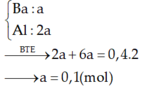
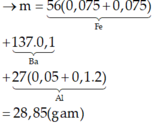
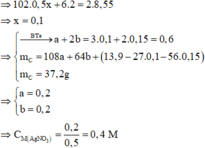



câu 1: C
câu 2:
M(OH)2 --> MO + H2O
M + 34 ........M +16
5,8 ..................4
=> 5,8(M+16) = 4(M+34)
=> 1,8M= 43,2
=> M=24 (Mg)
câu 3:
X + O2 => XO2
%X = \(\dfrac{X.100}{X+32}=50\)=> X =32 (S)
câu 4 : A
câu 5 :
Mg(NO3)2 + Ba(OH)2 ==> Mg(OH)2 + Ba(NO3)2
0,1 .................0.15
(hết)...............(dư)
=> nMg(OH)2 = 0,1
=> mMg(OH)2 = 5,8g
Câu 1: C.
Câu 2: Gọi KL mol của M là M
PTHH:
M(OH)2 --to--> MO + H2O
Theo đề ra, ta có:
nM(OH)2 = \(\dfrac{5,8}{M + 34}\)(mol)
nMO = \(\dfrac{4}{M+16}\)(mol)
Theo PT => \(\dfrac{5,8}{M + 34}\)= \(\dfrac{4}{M+16}\)
=> M = 24
Vậy M là Mg.
Câu 3:
X chiếm 50% KL.
=> %O = 50%
<=> MO = 32 = 50%
=> MX = 32
Vậy X là S.
Câu 4: A.
Câu 5:
V dd Ba(OH)2 bằng bao nhiêu bạn?
Nếu cùng bằng 100ml thì tính thế này:
nMg(NO3)2 = 1.0,1 = 0,1 (mol)
nBa(OH)2 = 1,5.0,1 = 0,15 (mol)
Mg(NO3)2 + Ba(OH)2 ----> Ba(NO3)2 + Mg(OH)2
Ta có tỉ lệ: \(\dfrac{0,1}{1}<\dfrac{0,15}{1}\)
=> Ba(OH)2 dư, Mg(NO3)2 hết
Theo PT, ta có: nMg(OH)2 = nMg(NO3)2 = 0,1 (mol)
=> mMg(OH)2 = 0,1.58 = 5,8 (g)