1/ X là hỗn hợp hai kim loại Mg và Zn. Y là dung dịch H2SO4 chưa rõ nồng độ.
Thí nghiệm 1: Cho 24,3g X vào 2 lít Y, sinh ra 8,96 lít khí H2.
Thí nghiệm 2: Cho 24,3g X vào 3 lít Y, sinh ra 1,12 lít khí H2.
(Các thể tích khí đều đo ở đktc)
a. Chứng tỏ rằng trong thí nghiệm 1 thì X chưa tan hết, trong thí nghiệm 2 thì X tan hết.
b. Tính nồng độ mol của dung dịch Y và khối lượng mỗi kim loại trong X.
2/ Tính nồng độ ban đầu của dung dịch H2SO4 và dung dịch NaOH biết rằng:
- Nếu đổ 3 lít dung dịch NaOH vào 2 lít dung dịch H2SO4 thì sau khi phản ứng dung dịch có tính kiềm với nồng độ 0,1M.
- Nếu đổ 2 lít dung dịch NaOH vào 3 lít dung dịch H2SO4 thì sau phản ứng dung dịch có tính axit với nồng độ 0,2M.
Làm ơn, giúp mik với. Mik đang cần gấp!


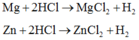

Câu 1:
Câu 2:
Gọi nồng độ của dung dịch H2SO4 và dung dịch NaOH lần lượt là: a,b (M)
2NaOH + H2SO4 => Na2SO4 + 2H2O
TH1: Sau pứ dung dịch có tính kiềm
=> NaOH dư
nH2SO4 = CM.V = 2a (mol)
nNaOH = CM.V = 3.b (mol)
Vdd = 2 + 3 = 5 (l)
Vì NaOH dư nên đặt số mol H2SO4 lên phương trình ta được số mol NaOH pứ = 4a (mol)
Theo đề bài ta có: 3b - 4a = 0.1x5 = 0.5 (1)
TH2: Sau pứ dung dịch có tính axit
=> H2SO4 dư
nH2SO4 = CM.V = 3a (mol)
nNaOH = CM.V = 2b (mol)
Vdd = 2 + 3 = 5 (l)
Vì H2SO4 dư nên ta đặt số mol NaOH lên pt => số mol H2SO4 pứ là: b (mol)
Theo đề bài ta có: 3a - b = 0.2 x 5 = 1 (2)
Từ (1) và (2) suy ra: a =0.7 ; b = 1.1
Vậy CM dd H2SO4 = 0.7 M
CM dd NaOH = 1.1 M .