Cho a(g) Al vào 100ml ddHcl 1M. Sau đó thấy b(g) rắn không tan, tiếp tục cho rắn đó vào 100ml đ NaOH !M thấy thoát ra 6,72l khí. Tìm a ( mọi người giúp e với ạ chiều nay e phải nộp rồi)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


vì có khí thoát ra ⇒Al dư
\(n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\\ n_{AgNO_3}=0,3.1=0,3mol\\ n_{CuSO_4}=0,2.1=0,2mol\)
\(Al+3AgNO_3\rightarrow3Ag+Al\left(NO_3\right)_3\)
0,1 0,3 0,3
\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
\(\dfrac{2}{15}\) 0,2 \(\dfrac{1}{15}\) 0,2
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,01 0,015
\(m_1=m_{Al}=\left(0,01+0,1+\dfrac{2}{15}\right)27=6,57g\)
\(m_2=0,01.27+0,3.108+0,2.64=45,47g\)

Chọn B.
Khi cho A vào H2O thì phần không tan B là FeO và có thể có Al2O3 dư. Cho B và CO dư thì thu được chất rắn E là Fe và có thể có Al2O3. Cho E vào NaOH dư thì bị tan một phần nên Al2O3 còn dư, chất rắn G là Fe.

Na2CO3 + HCl = NaCl + NaHCO3
KHCO3 + HCl = KCl +CO2 + H2O
n HCl = 0,1 * 1,5=0,15 mol
n CO2 = 1,008 / 22,4 =0,045 mol => n KHCO3 = 0,045 mol = n iôn K+ = n iôn HCO3 -=> nồng độ MOl
dd B tác dụng với Ba(OH)2 dư : Ba(OH)2 (dư) + NaHCO3 = BaCO3 + NaOH +H2O
n kết tủa= n BaCO3 = 29,55/197=0,15 mol => n NaHCO3 = 0,15 mol = nNa2CO3 => n Na + trong ddA = 0,15 *2 = 0,3 mol => nồng độ mol
nHCO3 - = 0,15 mol => nồng độ mol
Có n Na2CO3 và nKHCO3 dễ dàng tính được a(g)
**** Cho từ từ DD A gồm Na2CO3 và NaHCO3 va ddHCl thì sẽ có 2 trường hợp
TH1: Na2CO3 phản ứng trước:
Na2CO3 +2 HCl =2NaCl + H2O +CO2
.................0,15
n Na2CO3 ở câu trên tính dc là 0,15 mol => n HCl phản ứng ở đây là 0,15 * 2 = 0,3 mol

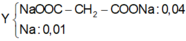


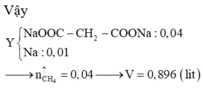
- nHCl = 0,1 mol
2Al + 6HCl ---> 2AlCl3 + 3H2 (1)
- b(g) chất rắn ko tan là Al dư
- Cho rắn đó vào NaOH
2Al + 2NaOH + 2H2O -----> 2NaAlO2 + 3H2 (2)
- nH2 = 0,3 mol
- Theo PTHH(2): nNaOH pư = 0,2 mol
( cho hỏi đề ở cái đoạn 100ml NaOH !M là 1M hay ?M vậy)
nồng độ mol của NaOH chưa biết hay biết rồi vậy
Cảm ơn bạn nha chỗ đó là 1M nhưng mik viết nhầm