Nung nóng 13,1g hỗn hợp gồm: Al, Zn, Mg, trong oxi vừa đủ thu được 20,3g oxit. Hoà tan hỗn hợp oxit trên cần dùng V(l) dung dịch HCl nồng độ 0,4M
a, Tính V
b, Tính khối lượng muối clorua tạo thành
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Bảo toàn khối lượng: m oxit + m HCl = m muối + m H 2 O
⇒ 20,3 + 0,9.36,5 = m muối + 0,45.18
⇒ m muối = 45,05g

\(a)m_{O_2}=20,3-13,1=7,2g\\ n_{O_2}=\dfrac{7,2}{32}=0,225mol\\ BTNT\left(O\right):n_{H_2O}=2n_{O_2}=0,225.2=0,45mol\\ BTNT\left(H\right):n_{HCl}=2n_{H_2O}=0,45.2=0,9mol\\ V_{HCl}=\dfrac{0,9}{0,4}=2,25l\\ b)BTKL:m_{oxit}+m_{HCl}=m_{muối}+m_{nước}\\ \Leftrightarrow20,3+0,9.36,5=m_{muối}+0,45.18\\ \Rightarrow m_{muối}=45,05g\)
P/s: giống bài lớp 9 vậy:)

Bài này cần dùng sơ đò chuyển hóa :
__________________________Bài làm ___________________________
Ta có sơ đò chuyển hóa :
\(Mg,Zn,Al\underrightarrow{+O2}MgO,ZnO,Al2O3\)
\(MgO,ZnO,Al2O3\underrightarrow{+HCl}MgCl2,ZnCl2,AlCl3\)
a) Ta có khối lượng của O2 đã phản ứng là :
mO2=20,3-13,1=7,2 g
Vậy => mO2 trong hh oxit là 7,2 g
mO2 trong nước thu được khi cho hh oxit tác dụng với HCl cũng bằng 7,2 g
=> nO2\(_{\left(trong-hh-\text{ox}it\right)}=nH2O\) = 7,2/16 = 0,45 ( mol)
=> nHCl=2nH2=2.0,45=0,9 mol
=> VHCl=\(\dfrac{n}{V}=\dfrac{0,9}{0,4}=2,25\left(lit\right)\)
VO2=0,45.22,4=10,08 (l)
b) áp dụng ĐLBTKL ta có :
mhh(oxit) + mHCl = m\(_{mu\text{ối}-clorua}+mH2O\)
=> m\(_{mu\text{ối}-clorua}=mhh\left(\text{ox}it\right)+mHCl-mH2O=20,3+0,9.36,5-0,45.1=45,05\left(g\right)\)
Nếu Viết PTHH thì bạn tự viết ra nhé rồi sau đó gọi chung hh kim loại và hh oxit là X và Y rồi viết pthh TQ sau :
X + O2 -> oxit
Y + HCl -> muối clorua + H2O

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Ta có khối lượng O 2 đã phản ứng : m O 2 = 20,3 - 13,1 = 7,2 (g)
Vậy khối lượng oxi trong hỗn hợp oxit là 7,2 gam.
Toàn bộ lượng oxi trong oxit đã chuyển vào H 2 O nên ta có m O ( H 2 O ) = 7,2g
Cứ 1 mol H 2 O thì chứa 1 mol nguyên tử O ⇒ n H 2 O = n O = 7,2 : 16 = 0,45 mol
Từ phương trình ta có:
n HCl = 2 n H 2 O = 2.0,45 = 0,9 mol
⇒ V HCl = 0,9/0,4 = 2,25l

a)
$m_{O\ trong\ oxit} = 40,6 - 26,2 = 14,4(gam)$
$n_O = \dfrac{14,4}{16} =0,9(mol)$
$2H^+ + O^{2-} \to H_2O$
$n_{HCl} = n_{H^+} = 2n_O = 1,8(mol)$
$\Rightarrow V = \dfrac{1,8}{0,5} = 3,6(lít)$
b) $n_{Cl} = n_{HCl} = 1,8(mol)$
$m_{muối} = m_{kim\ loại} + m_{Cl} = 26,2 + 1,8.35,5 = 90,1(gam)$

Bảo toàn khối lượng :
\(m_{O_2}=44.6-28.6=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.5=1\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2\cdot n_{H_2O}=2\cdot1=2\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{2}{1}=2\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=44.6+2\cdot36.5-1\cdot18=99.6\left(g\right)\)
\(n_O=\dfrac{44,6-28,6}{16}=1\left(mol\right)\)
\(n_{HCl}=n_{Cl^-}=n_O=2\left(mol\right)\)
\(m_{muối}=m_{KL}+m_{Cl^-}=28,6+2.35,5=99,6\left(g\right)\)
\(V_{HCl}=\dfrac{2}{1}=2\left(l\right)\)

Chọn C
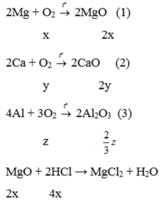

Áp dụng định luật bảo toàn khối lượng cho PT (1), (2), (3), ta có:
![]()
![]()
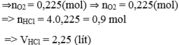

\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Gọi \(n_{Fe}=x\left(mol\right);n_{Zn}=y\left(mol\right)\)
\(Tacó:\left\{{}\begin{matrix}127x+136y=10,43\\2x+2y=0,5.0,4=0,2\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,35\\y=-0,25\end{matrix}\right.\)
Xem lại đề !
em có thể tiếp tục sân chơi được không? Cố lên ~~~ anh đi làm cv đây

\(a.\\ m+m_{\left[O\right]}=16,2\\ n_{Cl^-}=2\dfrac{m_{\left[O\right]}}{16}\\ m+35,5\dfrac{m_{\left[O\right]}}{16}\cdot2=38,2\\ m=9,8;m_{\left[O\right]}=6,4\\ b.\\ V_{dd.acid}=v\left(L\right)\\ n_{H^+}=v+v=2v\left(mol\right)\\ n_{\left[O\right]}=\dfrac{6,4}{16}=0,4=\dfrac{2v}{2}\\ v=0,4\\ a=9,8+0,4\cdot35,5+0,4\cdot96=62,4g\)
`a)`
Bảo toàn KL:
`m_Y+m_{HCl}=m_{\text{muối}}+m_{H_2O}`
`->36,5n_{HCl}-18n_{H_2O}=38,2-16,2=22`
Mà bảo toàn H: `n_{HCl}=2n_{H_2O}`
`->n_{HCl}=0,8(mol);n_{H_2O}=0,4(mol)`
Bảo toàn O: `n_{O(Y)}=n_{H_2O}=0,4(mol)`
`->n_{O_2}=0,5n_{O(Y)}=0,2(mol)`
Bảo toàn KL: `m_X+m_{O_2}=m_Y`
`->m=16,2-0,2.32=9,8(g)`
`b)`
Đặt `V_{dd\ ax it}=x(l)`
`->n_{HCl}=x(mol);n_{H_2SO_4}=0,5x(mol)`
`n_{O(Y)}=0,4(mol)`
Bảo toàn electron: `n_{O(Y)}=1/2n_{H(ax it)}`
`->0,4=1/2(x+0,5x.2)`
`->x=0,4(l)`
`->n_{HCl}=0,4(mol);n_{H_2SO_4}=0,2(mol)`
Bảo toàn O: `n_{H_2O}=n_{O(Y)}=0,4(mol)`
Bảo toàn KL:
`m_Y+m_{HCl}+m_{H_2SO_4}=m_{\text{muối}}+m_{H_2O}`
`->a=16,2+0,4.36,5+0,2.98-0,4.18=43,2(g)`
b) - Đặt CTHH tổng quát của oxit gồm 3 kim loại đó là \(X_2O_n\)
\(2X+\dfrac{n}{2}O_2\) ---to----> \(X_2O_n\) (1)
- Theo PTHH(1): nX = 2.\(n_{X_2O_n}\)
=> \(\dfrac{13,1}{X}=\dfrac{2.20,3}{2X+16n}\)
=> n = \(\dfrac{9}{131}X\)
\(X_2O_n+2nHCl\) ------> \(2XCl_n+\dfrac{n}{2}H_2O\) (2)
- Theo PTHH (2): \(n_{XCln}=2n_{X2On}\)
\(\Leftrightarrow\dfrac{m_{XCln}}{X+35,5n}=2.\dfrac{13,1}{2X}\)
\(\Leftrightarrow m_{XCln}=2.\dfrac{13,1}{2X}.\left(X+35,5n\right)\)
\(\Rightarrow m_{XCln}=2.\dfrac{13,1}{2X}.\left(X+35,5n\right)\)
Mà \(n=\dfrac{9}{131}X\)
=> mXCln = 45,05 gam