Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Bảo toàn khối lượng: m oxit + m HCl = m muối + m H 2 O
⇒ 20,3 + 0,9.36,5 = m muối + 0,45.18
⇒ m muối = 45,05g

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Ta có khối lượng O 2 đã phản ứng : m O 2 = 20,3 - 13,1 = 7,2 (g)
Vậy khối lượng oxi trong hỗn hợp oxit là 7,2 gam.
Toàn bộ lượng oxi trong oxit đã chuyển vào H 2 O nên ta có m O ( H 2 O ) = 7,2g
Cứ 1 mol H 2 O thì chứa 1 mol nguyên tử O ⇒ n H 2 O = n O = 7,2 : 16 = 0,45 mol
Từ phương trình ta có:
n HCl = 2 n H 2 O = 2.0,45 = 0,9 mol
⇒ V HCl = 0,9/0,4 = 2,25l

a)
$m_{O\ trong\ oxit} = 40,6 - 26,2 = 14,4(gam)$
$n_O = \dfrac{14,4}{16} =0,9(mol)$
$2H^+ + O^{2-} \to H_2O$
$n_{HCl} = n_{H^+} = 2n_O = 1,8(mol)$
$\Rightarrow V = \dfrac{1,8}{0,5} = 3,6(lít)$
b) $n_{Cl} = n_{HCl} = 1,8(mol)$
$m_{muối} = m_{kim\ loại} + m_{Cl} = 26,2 + 1,8.35,5 = 90,1(gam)$

Chọn C
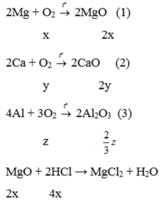

Áp dụng định luật bảo toàn khối lượng cho PT (1), (2), (3), ta có:
![]()
![]()
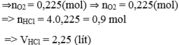

Bảo toàn khối lượng :
\(m_{O_2}=3.43-2.15=1.28\left(g\right)\)
\(n_{O_2}=\dfrac{1.28}{32}=0.04\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.04\cdot2=0.08\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2n_{H_2O}=2\cdot0.08=0.16\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{0.16}{0.5}=0.32\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muôi}=3.43+0.16\cdot36.5-0.08\cdot18=7.83\left(g\right)\)
Bảo toàn khối lượng:
m oxit = m kim loại + m O
=> mO = 3,43 – 2,15 = 1,28g
=> nO = 0,08 mol
Có nH+ = 2nO = 0,08 . 2 = 0,16 mol
V =\(\dfrac{0,16}{0,5}\)= 0,32 lít = 320ml
\(m_{muối}=m_{KL}+m_{Cl^-}=2,15+0,16.35,5=7,83\left(g\right)\)

1.
Trích một ít cả 2 chất vào nước
CaO + H2O \(\rightarrow\)Ca(OH)2 (bazo)
P2O5 + 3H2O \(\rightarrow\)2H3PO4 (axit)
sau đó cho quỳ tím vào nếu quỳ tím chuyển đỏ thì là axit,còn quỳ tím chuyển xanh thì là bazo
2.
Tổng hiệu suất khi sản xuất CaO bằng loại đá vôi là:
\(\dfrac{80.85}{100}=68\%\)
Số g CaO được sản xuất bằng 1 tấn đá vôi loại này là:
\(1\dfrac{68}{100}=0,68\left(tấn\right)=680kg\)

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

\(n_{Mg}=0,07mol;n_{Al}=0,08mol\\ n_{Cl_2}=a;n_{O_2}=b\\ 2H^++O^{2-}->H_2O\\ n_{H^+}=0,12\cdot\dfrac{2}{2}=2b\\ b=0,06mol\\ BTDT:0,07\cdot2+0,08\cdot3=2a+4b\\ a=0,07\\ \%V_{Cl_2}=\dfrac{a}{a+b}=53,85\%\)
Bài này cần dùng sơ đò chuyển hóa :
__________________________Bài làm ___________________________
Ta có sơ đò chuyển hóa :
\(Mg,Zn,Al\underrightarrow{+O2}MgO,ZnO,Al2O3\)
\(MgO,ZnO,Al2O3\underrightarrow{+HCl}MgCl2,ZnCl2,AlCl3\)
a) Ta có khối lượng của O2 đã phản ứng là :
mO2=20,3-13,1=7,2 g
Vậy => mO2 trong hh oxit là 7,2 g
mO2 trong nước thu được khi cho hh oxit tác dụng với HCl cũng bằng 7,2 g
=> nO2\(_{\left(trong-hh-\text{ox}it\right)}=nH2O\) = 7,2/16 = 0,45 ( mol)
=> nHCl=2nH2=2.0,45=0,9 mol
=> VHCl=\(\dfrac{n}{V}=\dfrac{0,9}{0,4}=2,25\left(lit\right)\)
VO2=0,45.22,4=10,08 (l)
b) áp dụng ĐLBTKL ta có :
mhh(oxit) + mHCl = m\(_{mu\text{ối}-clorua}+mH2O\)
=> m\(_{mu\text{ối}-clorua}=mhh\left(\text{ox}it\right)+mHCl-mH2O=20,3+0,9.36,5-0,45.1=45,05\left(g\right)\)
Nếu Viết PTHH thì bạn tự viết ra nhé rồi sau đó gọi chung hh kim loại và hh oxit là X và Y rồi viết pthh TQ sau :
X + O2 -> oxit
Y + HCl -> muối clorua + H2O