Một hỗn jowpj A gồm Al2O3, MgO được chia làm 2 phần bằng nhau mỗi phần có khối lượng 19.88 g
-TN1: Cho phần 1 tác dụng với 200ml dd HCl xM đến phản ứng hoàn toàn rồi cô cạn thu được 47.38 g chất rắn
-TN2: Cho phần 2 tác dụng với 400ml dd HCl trên đến phản ứng hoàn toàn rồi cô cạn thu được 50.68 g chất rắn
a) Tính x M
b)Tính khối lượng từng KL trong A

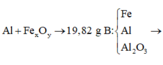




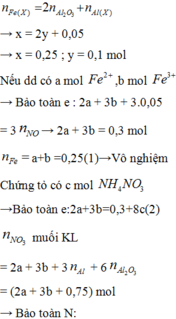
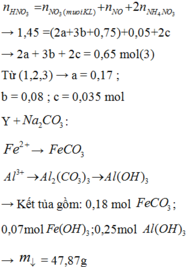
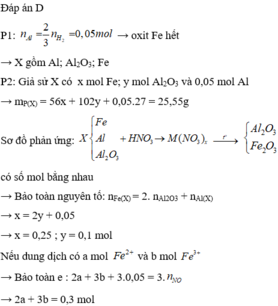

Vì khi thêm axit HCl mà khối lượng chất rắn tăng thêm nên chứng tỏ trong TN1 oxit phản ứng chưa hết.
Vì \(\dfrac{47,38}{50,68}>\dfrac{200}{400}\) => lượng axit ở TN2 đã phản ứng hết.
PTPƯ: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
x.........2x...........x
\(AI_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
y..........6y..........2y
Theo đề bài ta có hệ pt:
\(\left\{{}\begin{matrix}40x+102y=19,88\\95x+267y=50,68\end{matrix}\right.\Rightarrow x=0,14;y=0,14\)
Số mol HCl phản ứng phần 2: \(2x+6y=1,12\left(mol\right)\)
Số mol HCl phản ứng p1: \(\dfrac{47,38}{50,68}.1,12=1,047\left(mol\right)\)
Nồng độ mol dung dịch HCl: \(CM=\dfrac{1,047}{0,2}=5,235\left(M\right)\approx5\left(M\right)\)
\(\%m_{MgO}=\dfrac{0,14.40}{19,88}100\%=28,17\%;\%Al_2O_3=71,83\%\)
nHCl ở dòng 12 là sao nhỉ bn giải thích dk