hợp chất Z được tạo bởi 2 nguyên tố M và X có công thức MaXb .trong đo M chiếm 46,67% về khối lượng. trong hạt nhân nguên tử M có nM=pM+4, còn lại trong hạt nhân của X có nX=pX. Biết rằng tổng số hạt proton trong Z là 58 và a+b=3. Công thức phân tử của Z là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có : %M=46,67% => %X=53,33%
nM = pM + 4 ; nX= pX ; apM + bpX =58
Lại có : \(\frac{a\left(p_M+n_M\right)}{a\left(p_M+n_M\right)+b\left(p_X+n_X\right)}=46,67\%\) => \(\frac{a\left(p_M+n_M\right)}{2\left(ap_M+bp_X\right)+4}=46,67\%\)
=> a(pM+nM) = \(46,67\%\times[\left(2\times58\right)+4]\approx56\)
Tương tự ta có : b(pX+nX) = \(53,33\%\times[\left(2\times58\right)+4]\approx64\)
Theo bài ra ta có : a +b =3
=> +) Nếu a=2 => b=1 => M=56:2=28 ; X=64 (loại)
+) Nếu a=1 => b=2 => M 56 (Fe) ; X = 64:2=32 (S)
Vậy công thức phân tử Z là : FeS2

Gọi n, p là số notron và proton của M
n1, p1 là số notron và proton của R
Vì R chiếm 6,667% về khối lượng trong Z nên ta có :
\(\dfrac{b.\left(n_1+p_1\right)}{a\left(n+p\right)+b\left(n_1+p_1\right)}\)=6,667%
<=> 93,333b(n1+p1) - 6,667a(n+p) = 0 (1)
Tổng số proton trong phân tử Z là 84 :
=> ap + bp1 = 84(2)
Theo bài, ta có :
n = p + 4 (3)
n1 = p1 (4)
a + b =4 (5)
Từ (1)(3)(4) ta có PT: 186,666bp1 - 6,667a(2p+4) = 0 (6)
Vì a, b là các số nguyên dương và a + b =4
Nên ta có 3TH:
TH1: a=1 và b=3
TH2: a=b=2
TH3: a=3 và b=1
Thay a và b trong từng trường hợp trên vào PT (6) và PT(2) ta được hệ PT ẩn số p và p1( ĐK : p và p1 cũng là số nguyên dương)
=> Giải hệ chỉ có trường hợp (3) là thỏa mẵn với p= 26 và p1 = 6
p=26 => M = Fe
p1= 6 => R = C
Vậy công thức của Z là Fe3C

Chọn B
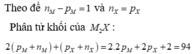
X chiếm 8/47 phần khối lượng => Nguyên tử khối X=16 và M=39
=> Số proton trong X là 8 (oxi), trong M là 19 (kali)
Hợp chất K 2 O có liên kết ion.

Đáp án B.
Theo đề nM - pM = 1 và nX = pX
Phân tử khối của M2X : 2(pM + nM) + (pX + nX) = 2.2pM + 2pX + 2 = 94
X chiếm 8/47 phần khối lượng => Nguyên tử khối X=16 và M=39
=> Số proton trong X là 8 (oxi), trong M là 19 (kali)
Hợp chất K2O có liên kết ion.

Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng → ZM + NM =
7
15
. (116 + NM- ZM ) → 22ZM + 8NM = 812
Ta có hệ
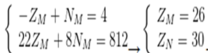
M là Fe
→ ZX =
58
-
26
2
= 16 → X là S
Công thức của A là FeS2.
Đáp án A.

Đáp án A
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM - ZM
M chiếm 46,67% về khối lượng
![]()
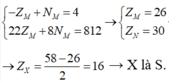
=> M là Fe

M chiếm 46,67% về khối lượng:

Quan sát – phân tích: Hệ 5 ẩn gồm 4 phương trình không thể giải thông thường để tìm nghiện vì ta cần phải rút gọn nghiệm: Phương trình (2) chứa ẩn ZM và x. ZA từ phương trình (1); (3); (4) ta có thể đưa về 1 phương trình chứa 2 ẩn ZM và x
Z A → Đưa về hệ phương trình 2 ẩn.
Ta đưa được về hệ sau
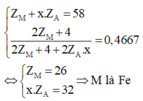
M là Fe nên x sẽ nhận giá trị từ 1 đến 3.
Từ x.ZA = 32 ta có các giá trị của ZA

Vậy H là FeS2
Đáp án A.
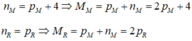
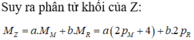
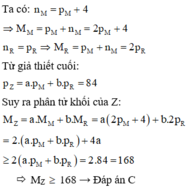
Ta có các hệ phương trình
nM=pm+4 (1)
nX=px (2)
a.pM +b.pX=58 (3)
\(\%M=\dfrac{a\left(p_M+n_M\right)}{a\left(p_M+n_M\right)+b\left(p_X+n_X\right)}.100\%=46,67\%\)(4)
Thay (1)(2) vào (4), ta được :
\(\%M=\dfrac{a\left(2p_M+4\right)}{a\left(2p_M+4\right)+b.2p_X}.100\%=46,67\%\) (5)
Từ (3)(5) và a+b=3
TH1: \(\left\{{}\begin{matrix}a=1\\b=2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p_M=26\\p_X=16\end{matrix}\right.\)=> M là Fe, X là S => CTPT Z: FeS2
TH2: \(\left\{{}\begin{matrix}a=2\\b=1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p_M=12,5\\p_X=33\end{matrix}\right.\)=> Loại vì không thõa điều kiện p,n,e nguyên
cái hệ 3 và 5 tính kiểu j vậy mn ?