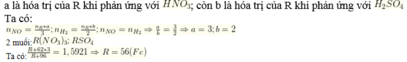khi hòa tan cùng 1 lượng kim loại R vào dd HNO3 {đ , t }và dd H2SO4 loãng ,thì thể tích NO2 thu đc gấp 3 lần thể tích H2 ở cùng đktc , khối lượng muối sunfat bằng 62, 89% khối lượng muối nitrat , tìm R
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà n N O 2 = 3 n H 2 n ê n n e n h ư ờ n g ( 1 ) = n N O 2 n e n h ư ờ n g ( 2 ) = 2 n H 2
Nên ne nhường(1) =3/2 ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
n e n h ư ờ n g ( 1 ) n e n h ư ờ n g ( 2 ) = n R . h o a t r i 1 n p . h o a t r i 2 = 3 2
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
m R S O 4 = 62 , 81 % m R ( N O 3 ) 2
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là: n NO2= 3nFe=9
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
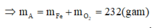
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:
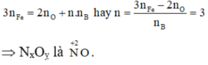
Khi đó:
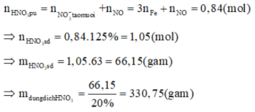

Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà nên
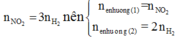
Nên ne nhường(1) = ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
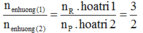
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
![]()
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là:
![]()
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
![]()
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử N + 5 nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:

Þ NxOỵ là .
Khi đó
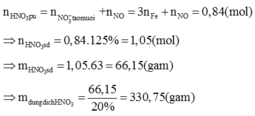

Gọi n, m là hóa trị của R khi tác dụng HNO3 và H2SO4 loãng ( 1≤ m≤ n≤ 3)
Chọn nR= 1 mol
2R + mH2SO4 →R2(SO4)m + mH2↑
1 → 0,5 0,5m
R + 2nHNO3 →R(NO3)n + nNO2 + nH2O
1 1 n
Ta có: n=3.0,5m n=1,5m m=2, n=3 là phù hợp.
Ta có: (R + 96)=(R + 186). 0,6281 R=56 R là Fe.
Đáp án B

Giả sử nNO2 = 3 mol và nH2 = 1 mol
TN1: Tác dụng với HNO3 đặc nóng
\(\text{n e = nNO2 = 3 mol}\)
Mà \(\text{nNO3-(muối KL) = n e = nNO2 = 3 mol}\)
\(\rightarrow\)m muối nitrat = mR + mNO3- = mR + 3.62 = mR + 186 (g)
TN2: Tác dụng với H2SO4 loãng
\(\text{n e = 2nH2 = 2 mol}\)
Mà \(\text{nSO4 2-(muối KL) = 0,5.n e = 1 mol}\)
=> m muối sunfat = mR + mSO4 2- = \(\text{mR + 1.96 = mR + 96 (g)}\)
Mà khối lượng muối sunfat bằng 62,8% khối lượng muối nitrat nên ta có:
\(m_R+96=\frac{62,8}{100}\left(mR+186\right)\rightarrow m_R=56\)
Giả sử hóa trị cao nhất của KL là n. Xét thí nghiệm 1:
Áp dụng bảo toàn e: n.nR = nNO2 → n.nR = 3 → nR = 3/n (mol)
→ MR = mR : nR = 56 : \(\frac{3}{n}\rightarrow M_R=\frac{56}{3}n\)
→ n = 3 và MR = 56 thỏa mãn
Vậy kim loại R là Fe

gọi số mol của Mg là a mol , Zn là b mol
=> 24a + 65b=21,4
nH2=1,1/2=0,55
Mg + H2SO4 --> MgSO4 +H2
a a mol
Zn + H2SO4 --> ZnSO4 +H2
b b mol
=> a + b = 0,55
=> a=0,35 mol ,b=0,2 mol
=> mMg = 0,35 *24=8,4 g
mZn =0,2 * 65= 13 g
mMgSO4 = 0,35 * 120=42
mZnSO4=0,2*161=32,2
=>m muối = 42 + 32,2=74,2 g
n H2SO4 = 0,35 + 0,2=0,55 mol
=>VH2SO4 = 0,55 *22,4=12,32 => V H2SO4 thực =12,32+ 12,32*10%=14,652 g

a, Ta có:
nZn = 13/65= 0,2(mol)
PTHH: Zn + H2SO4 → ZnSO4 + H2
0,2-----------------------------------0,2
Theo PT : nZnSO4 = 0,2.1/1 = 0,2(mol)
mZnSO4 = 0,2. 161 = 32,2(g)
b, Ta có:
Theo PT : nH2 = 0,2.1/1 = 0,2(mol)
VH2(đktc) = 0,2 . 22,4 = 4,48(l)
CuO+H2-to>Cu+H2O
0,2-----0,2
=>m Cu=0,2.64=12,8g
Cậu ơi cho tớ hỏi ngu tý là cái mà "0,2---------0,2" là ntn vậy ạ :"))?