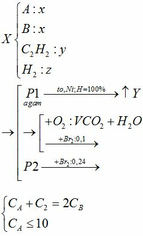
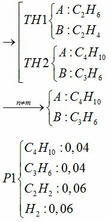
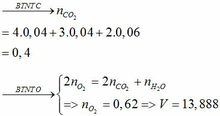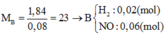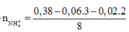Cho 144 ml dd H2SO4 96% (khối lượng riêng là 1,84 g/ml) và hỗn hợp khí A vào bình có dung tích 10 lít (đktc). Biết hỗn hợp khí A gồm không khí và một hidrocacbon X có công thức CnH2n+2 (n∈N*, n≥1), thể tích không khí trong A được lấy với lượng cần thiết vừa đủ để đốt cháy toàn bộ lượng hdrocacbon nới treen; giả thiết rằng thể tích không khí bao gồm 20% O2 và 80% N2. Hỗn hợp hợp khí A được đốt cháy trong bình trên đậy nắp kín. Kết thúc PƯ, làm lạnh để ngưng tụ hơi nước thấy số mol khí giảm 18,18% so với ban đầu.
a. Tìm công thức của hidrocacbon X và viết 1 phản ứng của khí X với khí Clo khi có ánh sáng.
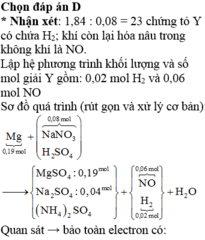
b. Xác định thành phần % theo thể tích của hỗn hợp khí A, của hỗn hợp khí sau PƯ.
c. Tính nồng độ % dd H2So4vaf tỉ lệ số mol H2SO4 : H2O sau khi kết thức thí nghiệm.