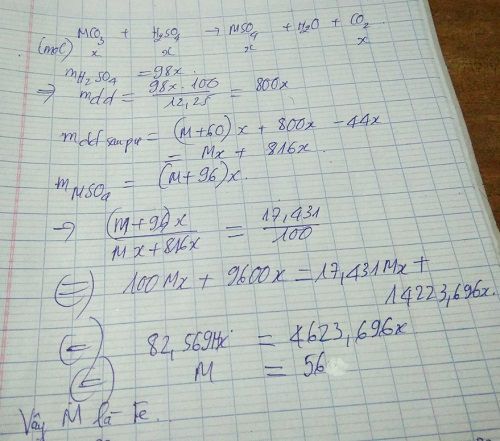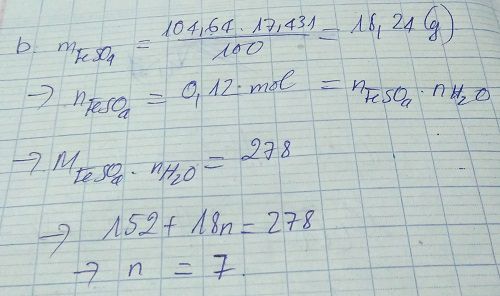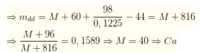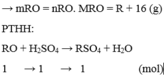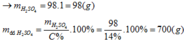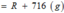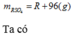Hoàn tan hoàn toàn muối RCO3 bằng một lượng vừa đủ dung dịch H2SO4 12,25% thu được dung dịch muối có nồng độ 17,431%
a.tìm loại R?
b. Cô cạn 122,88g dung dịch muối tạo thành ở trên làm bay bớt đi hơi nước và làm lạnh thu được 23,352g tinh thể muối .tìm công thức tinh thể muối . Biết hiệu suất của quá trình kết tinh muối là 70%