Cho phản ứng al + fe203 tạo ra hỗn hợp chất rắn
Chia chất rắn làm 2 phần = nhau
- phần 1 dd naoh dư tạo thành 33,6 lít khí h2 ở đktc
-phần 2: dd hcl dư tạo thành 44,8 lít h2 ở đktc
Tìm khối lượng fe203 và al tham gia pư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có sơ đồ phản ứng:
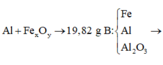
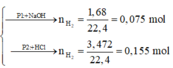
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
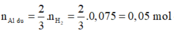
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
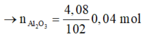
Ta có:
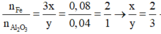
=> Oxit sắt cần tìm là Fe2O3

2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
n H 2 (p1) = 3,08/22,4 = 0,1375 mol
n H 2 (p2) = 0,84/22,4 = 0,0375 mol
Thấy phần 2 tác dụng với NaOH sinh ra khí, suy ra sản phẩm có Al dư.
Vậy rắn Y gồm A l 2 O 3 , Fe và Al dư.
Phần 2:
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2
Theo PTPU ta có:
n A l (p2) = 2/3 n H 2 (p2)
= 2/3 . 0,0375 = 0,025 mol
⇒ n A l (p1) = n A l (p2) = 0,025 mol
Phần 1:
Fe + H 2 S O 4 → F e S O 4 + H 2 (*)
2Al + 3 H 2 S O 4
→ A l 2 S O 4 3 + 3 H 2 (**)
Theo (**) ta có:
n H 2 (**) = 3/2 n A l (p1)
= 3/2 . 0,025 = 0,0375 mol
⇒ n H 2 (*) = n H 2 (p1) - n H 2 (**)
= 0,1375 - 0,0375 = 0,1 mol
⇒ n F e (p1) = n H 2 (*)=0,1 mol
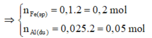
⇒ n A l pư = n F e sp = 0,2 mol
⇒ n F e 2 O 3 = 1/2 . n F e sp
= 1/2 . 0,2 = 0,1 mol
m h h = m F e 2 O 3 + m A l p u + m A l d u
= 0,1.160+0,05.27+0,2.27=22,75g
⇒ Chọn D.
Gọi a là số mol Al đã phản ứng, b là số mol Al dư
\(2Al\left(a\right)+Fe_2O_3\left(0,5a\right)-t^o->Al_2O_3\left(0,5a\right)+2Fe\left(a\right)\)
Vì chất rắn thu được tác dụng với dd NaOH tạo khí H2
Chứng tỏ Al dư sau phản ứng,
\(\Rightarrow C.răn:\left\{{}\begin{matrix}Fe:a\left(mol\right)\\Al_2O_3:0,5a\left(mol\right)\\Al\left(dư\right):b\left(mol\right)\end{matrix}\right.\)
Phần 1:
\(2NaOH+Al_2O_3\rightarrow2NaAlO_2+H_2O\)
\(2Al\left(0,5b\right)+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\left(0,75b\right)\)
\(n_{H_2}=1,5\left(mol\right)\)
\(\Rightarrow0,75b=1,5\left(I\right)\)
Phần 2:
\(Fe\left(0,5a\right)+2HCl--->FeCl_2+H_2\left(0,5a\right)\)
\(2Al\left(0,5b\right)+6HCl--->2AlCl_3+3H_2\left(0,75b\right)\)
\(Al_2O_3+6HCl--->2AlCl_3+3H_2O\)
\(n_{H_2}=2\left(mol\right)\)
\(\Rightarrow0,5a+0,75b=2\left(II\right)\)
Từ (I )và (II) \(\Rightarrow\left\{{}\begin{matrix}a=1\left(mol\right)\\b=2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}\left(bđ\right)=a+b=3\left(mol\right)\\n_{Fe_2O_3}=0,5a=0,5\left(mol\right)\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=81\left(g\right)\\m_{Fe_2O_3}=80\left(g\right)\end{matrix}\right.\)
bạn ơi cho mình hỏi 0,5b ở đâu ra vậy
giúp với