Trong phòng thí nghiệm người ta có thể điều chế khí oxi bằng cách đốt nóng Kali clorat KCLO3, sau phản ứng thu được chất rắn Kali clorid KCL và khí oxi
a) Viết phương trình hóa học xảy ra
b) Muốn điều chế được 6,72 lít khí oxi ( ở điều kiện tiêu chuẩn ) thì cần dùng bao nhiêu gam KCLO3 ?
c) Nếu có 1,5 mol KCLO3 tham gia phản ứng thì sẽ thu được bao nhiêu gam KCL và thể tích khí oxi ( ở điều kiện tiêu chuẩn ) là bao nhiêu lít ?

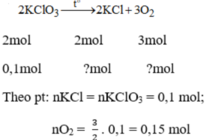
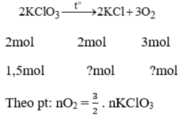
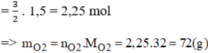
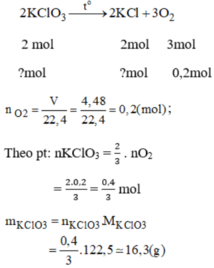
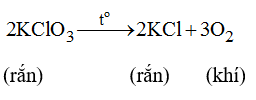

a) PTHH: 2KClO3 ----t°----> 2KCl + 3O2
b) nO2 = V / 22,4 = 6,72 / 22,4 = 0,3mol
nKClO3 = 2nO2 / 3 = 2 . 0,3 / 3 = 0,2mol
M KClO3 = 122,5g/mol
mKClO3 = n . M = 0,2 . 122,5 = 24,5g
c) nKCl = 2nKClO3 / 2 = 1,5mol
M KCl =74,5g
mKCl = n . M = 1,5 . 74,5 = 111,75g
nO2 = 3nKClO3 / 2 = 2,25mol
V O2 = n . 22,4 = 2,25 . 22,4 = 50,4l