Khử hoàn toàn 5,43g hỗn hợp CuO và PbO bằng khí H2 chất khí thu được dẫn qua bình đựng P2O5 thấy khối lượng bình tăng lên 0,9g.
a, Viết phương trình hóa học xayr ra.
b, Tính thành phần phần trăm theo khối lượng của mỗi oxit trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

khối lượng bình tăng lên là khối lượng H2O
nH2O=0,9/18=0,05 mol
goi x,y ll là số mol CuO và PbO
kê mol vào phương trình
ta có:80x+223y=5,43 (1); x+y=0,05 (2)
giải hpt 1 và 2 :x=0,04 mol; y=0,01 mol
%CuO=0,04.80.100/5,43=59%; %PbO=100-59=41%
PTHH: CuO + H2→ Cu + H2O (1)
PbO + H2→ Pb + H2O (2)
Sau phản ứng chất khí dẫn qua bình đựng P2O2 thấy khối lượng bình giảm 0,9 gam =>mH20 = 0,9 gam => nH20 = 0,9 /18 = 0,05 mol
Gọi số mol CuO và PbO lần lượt là x mol và y mol (x,y > 0)
Ta có PTĐS: 80x + 223y = 5,43 =>
Theo PTHH (1) ta có: nH20 = nCuO= x mol
Theo PTHH (2) ta có: nH2O = nPbO = y mol
x + y = 0,05 => y = 0,05 – x (b)
Thay (b) vào (a) giai ra ta có x = 0,04; y = 0,01 mol
Vậy % theo khối lượng của CuO và PbO là 59%; 40,06%
tớ giải rùi đó .Nhớ tick nhé![]()
![]()

a.PTHH: CuO + H2→ Cu + H2O (1)
PbO + H2→ Pb + H2O (2)
Sau phản ứng chất khí dẫn qua bình đựng P2O2 thấy khối lượng bình giảm 0,9 gam =>mH20 = 0,9 gam => nH20 = 0,9 /18 = 0,05 mol
Gọi số mol CuO và PbO lần lượt là x mol và y mol (x,y > 0)
Ta có PTĐS: 80x + 223y = 5,43 =>
b.Theo PTHH (1) ta có: nH20 = nCuO= x mol
Theo PTHH (2) ta có: nH2O = nPbO = y mol
x + y = 0,05 => y = 0,05 – x (b)
Thay (b) vào (a) giai ra ta có x = 0,04; y = 0,01 mol
Vậy % theo khối lượng của CuO và PbO là 59%; 40,06%

Phương trình :
CuO + H2 => Cu + H2O
Khối lượng bình tăng lên 0,9g => \(m_{H_2O}=0,9\left(g\right)\)
=> \(n_{H_2O}=\dfrac{0,9}{18}=0,05\left(mol\right)\)
Theo pt: \(nH_2O=nCuO=\dfrac{8}{80}=0,1\left(mol\right)\)
Vậy hiệu suất phản ứng là : H = \(\dfrac{0,05}{0,1}=50\%\)

PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
Ta có: \(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)=n_{CH_4}\)
Đặt \(\left\{{}\begin{matrix}n_{C_2H_4}=a\left(mol\right)\\n_{C_2H_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow a+b=\dfrac{5,04}{22,4}-0,075=0,15\) (1)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Theo PTHH: \(28a+26b=4,1\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{C_2H_4}=0,1\left(mol\right)\\b=n_{C_2H_2}=0,05\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(n_{hh}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,075}{0,225}\cdot100\%\approx33,33\%\\\%V_{C_2H_4}=\dfrac{0,1}{0,225}\cdot100\%\approx44,44\%\\\%V_{C_2H_2}=22,23\%\end{matrix}\right.\)

Gọi $n_{CuO} = a; n_{PbO} = b$
Ta có :
$80a + 223b = 15,15(1)$
$CuO + CO \xrightarrow{t^o} Cu + CO_2$
$PbO + CO \xrightarrow{t^o} Pb + CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Theo PTHH :
$n_{CO_2} = a + b = \dfrac{10}{100} = 0,1(2)$
Từ (1)(2) suy ra a = b = 0,05
Vậy :
$m_{CuO} = 0,05.80 = 4(gam)$
$m_{PbO} = 0,05.223 = 11,15(gam)$

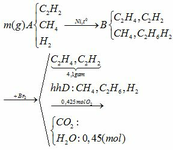
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)

Đáp án A
Hỗn hợp chứa axetilen, etilen và chất A khi đốt thu được CO2 và H2O tỉ lệ 1:1 thì chất A chắc chắn phải là ankan (do axetilen đốt thu được nCO2 > nH2O, etilen đốt thu được nCO2=nH2O, cần phải có 1 chất đốt thu được nCO2< nH2O để đảm bảo tỉ lệ)
Hơn nữa, nC2H2=nA
Khí thoát ra khỏi bình là ankan:
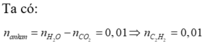
Khối lượng bình tăng lên là khối lượng của axetilen và etilen.

a)PTHH:CuO+H2\(\underrightarrow{t^0}\)H2O+Cu(1)
PbO+H2\(\underrightarrow{t^0}\)H2O+Pb(2)
3H2O+P2O5\(\underrightarrow{ }\)2H3PO4
b) Do bình tăng lên 0,9 gam. Do đó:\(m_{H_2O}=0,9\left(gam\right)\)
Gọi khối lượng của CuO là x(o<x<5,43)
khối lương của PbO là 5,43-x
Theo PTHH(1):80 gam CuO tạo ra 18 gam H2O
Vậy:x gam CuO tạo ra \(\frac{9x}{40}\) gam H2O(3)
Theo PTHH(2):223 gam PbO tạo ra 18 gam H2O
Vậy:5,43-x gam PbO tạo ra \(\frac{18\left(5,43-x\right)}{223}\) gam H2O(4)
Từ (3) vfa (4) ta có PT:\(\frac{9x}{40}\)+\(\frac{18\left(5,43-x\right)}{223}\)=0,9
\(\Rightarrow x=3,2\left(gam\right)\)
\(\Rightarrow m_{CuO}=3,2\left(gam\right);m_{PbO}=5,43-3,2=2,23\left(gam\right)\)
Do đó:\(\%m_{CuO}=\frac{3,2}{5,43}.100\%=58,93\left(\%\right)\)
\(\%m_{PbO}=100\%-58,93=41,07\left(\%\right)\)
CuO+H2\(\rightarrow\)Cu+H2O(1)
PbO+H2 \(\rightarrow\)Pb+H2O(2)
P2O5+3H2O\(\rightarrow\) 2H3PO4(3)
Theo PT(3) có: vì đây là phản ứng hóa hợp nên khối lượng mà bình tăng thêm=mH2O=0,9g
nH2O(pt1+pt2)=\(\dfrac{0,9}{18}\)=0,05mol
Gọi nH2(pt1)=a
nH2(pt2)=b
=> a+b=0,05 <=> b=0,05-a
Theo PT1: nCuO=nH2(PT1)=a
Theo PT2:nPbO=nH2(pt2)=b
Có mCuO+mPbO=5,43g
=>80a+223b=5,43
=>80a+223(0,05-a)=5,43
=>80a+11,15-223a=5,43
=>143a=5,72
=>a=0,04 mol
=> mCuO=0,04.80=3,2g
=>C%CuO=\(\dfrac{3,2}{5,43}\).100%=59%
C%PbO=100%-59%=41%