Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Đặt \(\left\{{}\begin{matrix}n_{Fe\left(oxit\right)}=a\left(mol\right)=n_{H_2}\\n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có: \(m_{tăng}=m_{Fe}-m_{H_2}\) \(\Rightarrow56a-2a=3,24\) \(\Rightarrow a=n_{Fe}=0,06\left(mol\right)\)
Hỗn hợp D gồm \(\left\{{}\begin{matrix}n_{CO_2\left(dư\right)}=c\left(mol\right)\\n_{H_2O}=n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}c+b=0,1\\18b+2c=7,4\cdot2\cdot\left(b+c\right)\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}b=0,08\\c=0,02\end{matrix}\right.\)
\(\Rightarrow x:y=a:b=0,06:0,08=3:4\)
\(\Rightarrow\) Công thức cần tìm là Fe3O4

Gọi số mol H2, O2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{22,4}{22,4}=1\\M_B=\dfrac{2a+32b}{a+b}=5,5.2=11\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,7 (mol); b = 0,3 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,7}{2}>\dfrac{0,3}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
0,6<--0,3------->0,6
=> \(\left\{{}\begin{matrix}m_{H_2O}=0,6.18=10,8\left(g\right)\\m_{H_2\left(dư\right)}=\left(0,7-0,6\right).2=0,2\left(g\right)\end{matrix}\right.\)

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

Gọi số mol CO2, CO trong khí C là a, b (mol)
Bảo toàn C: a + b = \(n_{CO\left(bđ\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Có: \(\overline{M}_C=\dfrac{44a+28b}{a+b}=18.2=36\left(g/mol\right)\)
=> a = 0,15 (mol); b = 0,15 (mol)
mCu = 1,92 (g)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
=> mCuO = 0,03 (mol)
=> mMxOy = 9,36 - 0,03.80 = 6,96 (g)
Có: nO(oxit) = nCO(pư) = nCO2
=> \(y.n_{M_xO_y}+0,03=0,15\)
=> \(n_{M_xO_y}=\dfrac{0,12}{y}\left(mol\right)\)
=> \(M_{M_xO_y}=x.M_M+16y=\dfrac{6,96}{\dfrac{0,12}{y}}=58y\left(g/mol\right)\)
=> \(M_M=21.\dfrac{2y}{x}\left(g/mol\right)\)
Xét \(\dfrac{2y}{x}=1\) => Loại
Xét \(\dfrac{2y}{x}=2\) => Loại
Xét \(\dfrac{2y}{x}=3\) => Loại
Xét \(\dfrac{2y}{x}=\dfrac{8}{3}\) => MM = 56 (g/mol)
=> M là Fe
\(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
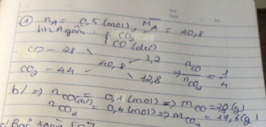


Thiếu đề
tui sửa lại rồi đó