

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(Z=1\Rightarrow1s^1\)
\(Z=2\Rightarrow1s^2\)
\(Z=3\Rightarrow1s^22s^1\)
\(Z=4\Rightarrow2s^22s^2\)
\(Z=5\Rightarrow1s^22s^22p^1\)
\(Z=6\Rightarrow1s^22s^22p^2\)
\(Z=7\Rightarrow1s^22s^22p^3\)
\(Z=8\Rightarrow1s^22s^22p^4\)
\(Z=8\Rightarrow1s^22s^22p^4\)
\(Z=9\Rightarrow1s^22s^22p^5\)
\(Z=10\Rightarrow1s^22s^22p^6\)
\(Z=11\Rightarrow1s^22s^22p^63s^1\)

Z = 1: 1s1
Z = 2: 1s2
Z = 3: 1s22s1
Z = 4: 1s22s2
Z = 5: 1s22s22p1
Z = 6: 1s22s22p2
Z = 7: 1s22s22p3
Z = 8: 1s22s22p4
Z = 9: 1s22s22p5
Z = 10: 1s22s22p6
Z = 11: 1s22s22p63s1
Z = 12: 1s22s22p63s2
Z = 13: 1s22s22p63s23p1
Z = 14: 1s22s22p63s23p2
Z = 15: 1s22s22p63s23p3
Z = 16: 1s22s22p63s23p4
Z = 17: 1s22s22p63s23p5
Z = 18: 1s22s22p63s23p6
Z = 19: 1s22s22p63s23p64s1
Z = 20: 1s22s22p63s23p64s2

Từ Z = 3 đến Z = 10 ta có các nguyên tử :
Li: 1 s 2 2 s 1 ; Be: 1 s 2 2 s 2 ; B: 1 s 2 2 s 2 2 p 1 ; C: 1 s 2 2 s 2 2 p 2
N: 1 s 2 2 s 2 2 p 3 ; O: 1 s 2 2 s 2 2 p 4 ; F: 1 s 2 2 s 2 2 p 5 ; Ne: 1 s 2 2 s 2 2 p 6
Nhận xét : Số electron thuộc lớp ngoài cùng của các nguyên tử đó tăng dần từ 1 (Li) đến 8 (Ne).

Cấu hình: 1s22s22p63s23p63d74s1
=> Z= 26 (Sắt - Fe)

a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
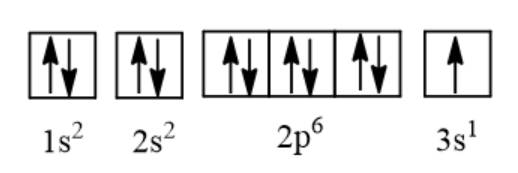
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA

Cấu hình electron của Al, Mg, Na, Ne :
Al 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 |
Mg 1 s 2 2 s 2 2 p 6 3 s 2 |
Na 1 s 2 2 s 2 2 p 6 3 s 1 |
Ne 1 s 2 2 s 2 2 p 6 |
Từ các cấu hình trên ta dễ dàng thấy rằng nếu :
nguyên tử Na nhường le để trở thành ion Na + ;
nguyên tử Mg nhường 2e để trở thành ion Mg 2 + ;
nguyên tử Al nhường 3e để trở thành ion Al 3 + ,
thì các ion được hình thành có cấu hình electron giống cấu hình electron của khí hiếm Ne với 8 electron ở lớp ngoài cùng.
Ta đã biết cấu hình electron của các khí hiếm với 8 electron (đối với He là electron) ở lớp ngoài cùng là một cấu hình electron vững bền. Vì vậy, các nguyên tử kim loại có khuynh hướng dễ nhường electron để có cấu hình electron vững bền của khí hiếm đứng trước.

Ứng với Z = 11, nguyên tử có 11 electron, do đó có cấu hình electron : 1 s 2 2 s 2 2 p 6 3 s 1
Nguyên tử có 3 lớp electron (lớp K, L, M), vậy nguyên tố đó thuộc chu kì 3. Lớp ngoài cùng có 1 electron, vậy nguyên tố đó thuộc nhóm IA. Các nguyên tố thuộc nhóm này (trừ hiđro) có tên chung là các kim loại kiềm.