Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH là: 2Al + H2SO4 → Al2(SO4) + H2.
Tỉ lệ giữa số nguyên tử Al lần lượt với số phân tử của ba chất trong phản ứng đều là 2:1
b) nAl =27/27 = 1 (mol)
theo PTHH ta có: số mol của H2SO4 = 1/2 * nAl = 1/2*1 =0.5 (mol)
khối lượng của H2SO4 là: 0.5 * (1*2+32+16*4) =49 (g).

1. CẤU TẠO PHÂN TỬ
– CTPT: H2SO4
– CTCT:
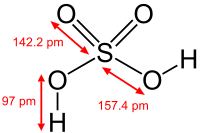
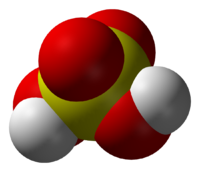

Trong hợp chất H2SO4, nguyến tố S có số oxi hoá cực đại là +6.
2. TÍNH CHẤT VẬT LÍ

– là chất lỏng, không màu, sánh như dầu, không bay hơi.
– H2SO4 98% có D= 1,84 g/cm3; nặng gần gấp 2 lần nước.
– H2SO4 đặc rất hút ẩm -> dùng làm khô khí ẩm.
– H2SO4 đặc tan vô hạn trong nước và toả nhiều nhiệt.
Giảithích hiện tượng thí nghiệm? Từ đó rút ra cách pha loãng axit sunfuric đặc?
– Khi pha loãng axit sunfuric đặc thì rót từ từ axit vào nước và khuấy nhẹ; không làm ngược lại ( nguy hiểm) (Tại sao?)
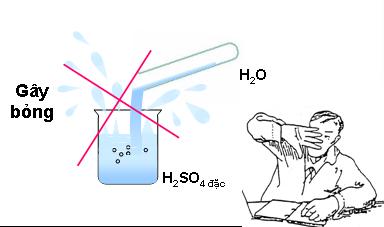
– Axit sunfuric đặc gây bỏng rất nặng -> cẩn thận khi làm thí nghiệm với axit sunfuric đặc
cô gái bị bỏng axit
3. TÍNH CHẤT HOÁ HỌC
a. Tính chất của axit sunfuric loãng
– Tính axit mạnh. Axit tác dụng được với chất nào?
+ Làm quì tím hoá đỏ
+ Tác dụng với muối (điều kiện: sản phẩm kết tủa hoặc bay hơi)
+ Tác dụng với oxit bazơ hoặc bazơ -> muối + H2O
+ Tác dụng kim loại trước hiđro ->muối hoá trị thấp của KL + H2
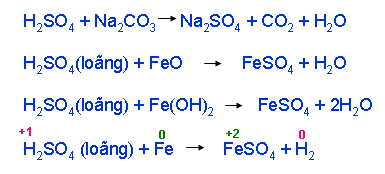
b. Tính chất của axit sunfuric đặc
Cu + H2SO4 loãng -> không phản ứng
Cu + H2SO4 đặc -> có xảy ra phản ứng không?
Nhận xét hiện tượng? Ngoài tính axit mạnh như axit sunfuric loãng thì axit sunfuric đặc còn có tính chất gì?
– Ngoài tính axit mạnh như axit sunfuric loãng thì axit sunfuric đặc còn có tính chất đặc trưng sau:
b.1. Tính oxi hoá mạnh
+ Tác dụng với kim loại ( hầu hết kim loại trừ Au, Pt)
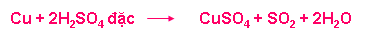

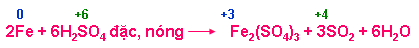
+ Tác dụng với phi kim ( C, S, P)
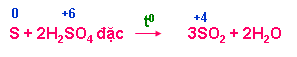
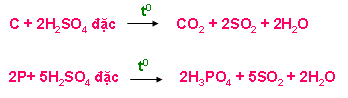
+ Tác dụng với hợp chất có tính khử ( HI, KI, KBr, FeO, Fe3O4, Fe(OH)2, FeCO3, H2S, …)
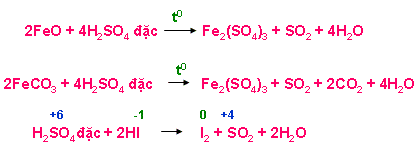
Nhỏ axit sunfuric đặc vào giấy
 Nhận xét hiện tượng? Suy ra axit sunfuric đặc còn có tính chất gì?
Nhận xét hiện tượng? Suy ra axit sunfuric đặc còn có tính chất gì?
b.2. Tính háo nước
– Axit H2SO4 đặc chiếm nước kết tinh của nhiều muối hiđrat (muối ngậm nước) hoặc chiếm các nguyên tố H và O (thành phần của nước) trong nhiều hợp chất
+ Hợp chất cacbohiđrat (Cn(H2O)m)
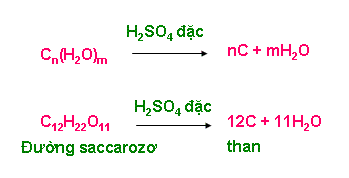
+ CuSO4.5H2O
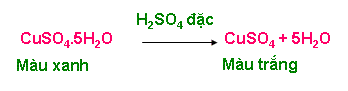
Phim thí nghiệm tính háo nước
Nhận xét hiện tượng? Vận dụng kiến thức trên, em hãy giải thích hiện tượng?
4. ỨNG DỤNG
– Hàng năm, thế giới sản xuất khoảng 160 triệu tấn H2SO4. Axit sunfuric là hoá chất hàng đầu trong nhiều ngành sản xuất như: phẩm nhuộm, luyện kim, chất dẻo, chất tẩy rửa, giấy sợi, sơn, phân bón, …
5. Sơ đồ sản xuất axit sunfuric
Click vào đây xem mô phỏng qui trình sản xuất
– Phương pháp tiếp xúc, gồm 3 công đoạn chính
a) Sản xuất SO2
– Từ quặng pirit sắt (FeS2)
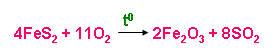
– Từ lưu huỳnh
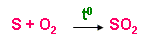
b) Sản xuất SO3
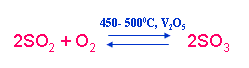
c) Sản xuất H2SO4
Dùng H2SO4 98% hấp thụ SO3 được oleum H2SO4.nSO3
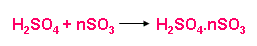
Dùng lượng nước thích hợp để pha loãng oleum, được H2SO4 đặc
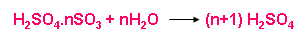

n Fe = \(\frac{4,2}{56}\)= 0.075 mol
\(PTHH:\text{Fe + H2SO4 -> FeSO4 + H2}\)
\(\Rightarrow\text{n Axit = n Fe = 0.075}\)
\(\Rightarrow\text{m axit = 0,075 . 98=7,35}\)
\(\Rightarrow\text{V H2 = 0,075 . 22,4=1,68l}\)

N2: là khí ,o màu; nhiệt độ nóng chảy là -209,86 oC, nhiệt độ sôi là -195,8oC
H2O: là chất lỏng, trong suốt, nhiệt độ sôi là 100oC
còn HCl thì mình o biết
N2 : loại khí cần thiết cho sự sống, chiếm phần lớn không khí Trái Đất.
H2O: Là phân tử gồm hiđro và oxi, cần thiết cho sự sống
HCl: Một loại axit

2) Kẽm + dd Axit clohidric ---> kẽm clorua + khí hidro
Zn + 2HCl ---> ZnCl2 + H2
BTKL: mZn + 6 = 13 + 7 ---> mZn = 14 g
1 , a , Axit sunfuric + natri hidroxit -> natri sunfat + nước

Do nguyên tử khối bằng 98 nên ta có phương trình
\(2+32x+16.4=98\)
\(\Leftrightarrow32x+66=98\Leftrightarrow32x=32\Leftrightarrow x=1\)
Vậy CTHH của axit đó là H2SO4
Vì PTK của \(H_2S_xO_4\)là 98 đvC nên ta có:
\(1.2+32.x+16.4=98\)
\(\Rightarrow\)\(2+32x+64=98\)
\(\Rightarrow\)\(32x=32\)
\(\Rightarrow\)\(x=1\)
CTHH của axit là \(H_2SO_4\)

a) Hợp chất H2S gồm 2 nguyên tố là H và S
Trong đó gồm 2 nguyên tử H và 1 nguyên tử O
Nguyên tử khôi = 2+32=34đvc
b) Hợp chất Al(OH)3 gồm 3 nguyên tố Al, O và H
Trong đó có 1 nguyên tử Al, 3 nguyên tử O và 3 nguyên tử H
Nguyên tử khối=27 +16.3+3=78đvc
c)Hợp chất CaO gồm 2 nguyên tố là Ca và O
Trong đó có 1 nguyên tử Ca và 1 nguyên tử O
Nguyên tử khối = 40+16=56đvc
d)Hợp chất H2SO4 gồm 2 nguyên tố là H , S vàO
Trong đó có 2 nguyên tử H, 1 nguyên tử S và 4 nguyên tử O
Nguyên tử khối = 2+32+16.4=98đvc

bài 2 :
a) nhợp chất = V/22.4 = 1/22.4= 5/112 (mol)
=> Mhợp chất = m/n = 1.25 : 5/112 =28 (g)
b) CTHH dạng TQ là CxHy
Có %mC = (x . MC / Mhợp chất).100%= 85.7%
=> x .12 = 85.7% : 100% x 28=24
=> x=2
Có %mH = (y . MH/ Mhợp chất ) .100% = 14,3%
=> y.1=14.3% : 100% x 28=4
=> y =4
=> CTHH của hợp chất là C2H4
Bài 1.
- Những chất có thể thu bằng cách đẩy không khí là : Cl2,O2,CO2 do nó nặng hơn không khí
- Để thu được khí nặng hơn không khí ta đặt bình đứng vì khí đó nặng hơn sẽ chìm và đẩy không khí ra bên ngoài
- Đẻ thu được khí nhẹ hưn thì ta đặt bình úp vì khí đó nhẹ hơn cho nen nếu đặt đứng bình thì nó sẽ bay ra ngoài

1) SO2 do 2 nguyên tố là S và O tạo ra
Có 1 nguyên tử S và 2 nguyên tử O trong 1 phân tử
Phân tử khối bằng : 32 + 16 x 2 = 32 + 32 = 64 ( đvC)
2) H2SO4 do 3 nguyên tố là H , S và O ( hoặc do 1 nguyên tố H và nhóm nguyên tử SO4 ) tạo thành
Có 2 nguyên tử H , 1 nguyên tử S và 4 nguyên tử O trong 1 phân tử
Phân tử khối bằng : 1 x 2 + 32 + 16 x 4 = 2 + 32 + 64 = 98 (đvC)
-H2SO4 là hợp chất đc tạo nên từ 3 nguyên tố là H,S,O
-Trong phân tử có 2 nguyên tử Hidro liên kết với 1 ng tử S liên kết với 1 ng tử Oxi
-PTK:H2SO4= 2NTK:H + NTK:S + 4NTK:O=98(đơn vị cacbon) (đvc)