
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trong các đơn chất halogen, chất điều kiện thường ở trạng thái rắn là I 2 .
Chọn đáp án D.

Đặc điểm hợp chất ion:
+ Các hợp chất ion thường là tinh thể rắn ở điều kiện thường
+ Hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi rất cao
=> Phát biểu (b) và (c) đúng

- Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn
- Mà astatine đứng dưới cùng trong nhóm halogen
=> Astatine tồn tại ở thể rắn trong điều kiện thường
- Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van dể Waals

Hầu hết các halogen đều là chất khí ở điều kiện thường trừ :
Br2 dạng lỏng ; I2 dạng rắn

Trong nhóm halogen đi từ trên xuống dưới, khối lượng phân tử và bán kính nguyên tử tăng
=> Lực tăng tác van der Waals tăng
=> Nhiệt độ sôi tăng
=> Astatine trong điều kiện thường tồn tại ở thể rắn

Đáp án C
S là chất rắn
H 2 S , O 2 là chất khí
H 2 SO 4 là chất lỏng

H2O ở thể lỏng, trong khi các hợp chất của hiđro khác như BH3, CH4, NH3, H2S, ... đều ở thể khí, vì các phân tử nước hút nhau bằng liên kết hiđro rất mạnh, làm cho các phân tử nước liên kết chặt chẽ. (Còn ở BH3, CH4 chúng không có liên kết hiđro, nên các phân tử không thể liên kết được với nhau).
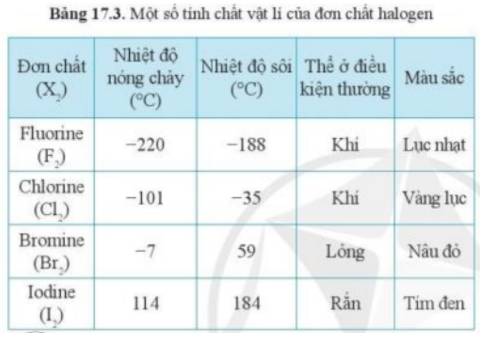
- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh