Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Vì V3 là lớn nhất nên dung dịch (2), (3) là hai axit Þ (1) là dung dịch chứa muối nitrat.
Phương trình ion: 4H+ + NO3- + 3e → NO + 2H2O

Chọn đáp án C
Do thu được số mol CO2 khác nhau ở 2 thí nghiệm ⇒ H+ không dư.
Xét thí nghiệm 1: nhỏ từ từ X vào Y thì xảy ra phản ứng theo thứ tự:
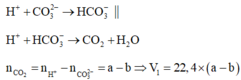
Xét thí nghiệm 2: nhỏ từ từ Y vào X thì xảy ra phả ứng
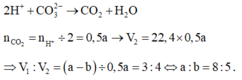

Đáp án D
nH+ (1) = nH+ (2) ⇒ 4V1 = V2 (3+1.2) ⇒V1 = 1,25V2

Đáp án D
Khi cho BaCl2 vào dung dịch B thì kết tủa thu được chỉ chứa BaSO4 → nBaSO4 = 0,18 mol
Bảo toàn nhóm SO42- → nCr2(SO4)3 = 0,18 : 3 = 0,06 mol → V2 = 0,06 : 0,5 = 0,12 lít
Ta có nCrCl3 = 0,12. 1 = 0,12 mol
Có dd A chứa 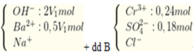
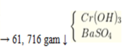
TH1: Nêu 0,5V1 > 0,18 → V1 > 0,36 lít thì kết tủa thu được chứa BaSO4 : 0,18 mol
→ nCr(OH)3 = 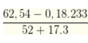 = 0,2 mol
= 0,2 mol
Vì nCr(OH)3 < nCr3+ → xảy ra sự hòa tan kết tủa tạo CrO2- : 0,24- 0,2 = 0,04 mol
Có nOH- = 3nCr(OH)3 + 4nCrO2- = 3. 0,2 + 4. 0,04 = 0,76 mol → V1 = 0,38 lít.
TH2: Nếu 0,5V1 < 0,18 → V1 < 0,36 lít.
Có nOH- = 2V1 < 0,72
→
n
O
H
-
n
C
r
3
+
<
0
,
72
0
,
24
=3 -> Cr(OH)3 chưa bị hòa tan kết tủa
Khi đó BaSO4 : 0,5V1 mol, Cr(OH)3 chưa bị hòa tan kết tủa
→ nCr(OH)3 =
n
O
H
-
3
m
o
l
=
0
,
2
V
1
3
→ 62,54 = 0,5V1. 233 +
0
,
2
v
1
3
. 103 → V1 = 0,337 lít
Vậy thể tích ít nhất cần dùng là 0,337 lít.

Đáp án C
Chất tan duy nhất là Na2SO4 do đó: 0,4V1=0,6V2.2 suy ra V1=3V2.
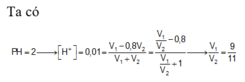

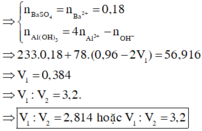


Để thu được dung dịch có pH = 2 chứng tỏ dung dịch sau phản ứng chứa axit dư [H+] dư = 0,01 M
→ nH+(du) = 0,04V1-0,035V2 = 0,01.(V1 + V2) → 0,03V1 = 0,045V2 → V1 : V2 = 3:2
Đáp án B