
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{NaOH}=0,02.2=0,04\left(mol\right)\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ a.n_{H_2SO_4}=n_{Na_2SO_4}=\dfrac{0,04}{2}=0,02\left(mol\right)\\ C_{MddH_2SO_4}=\dfrac{0,02}{0,08}=0,25\left(M\right)\\ b.\left[Na^+\right]=\dfrac{0,02.2}{0,02+0,08}=0,4\left(M\right)\\ \left[SO^{2-}_4\right]=\dfrac{0,02}{0,02+0,08}=0,2\left(M\right)\)

\(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\\ n_{CH_3COOH}=\dfrac{m}{60}\left(mol\right)\\ n_{NaOH}=n_{CH_3COOH}=\dfrac{m}{60}\left(mol\right)\\ \Rightarrow V_{NaOH}=\dfrac{\dfrac{m}{60}}{1}=\dfrac{m}{60}\left(l\right)=\dfrac{50m}{3}\left(ml\right)\)

nKOH = 0,25 . 2 = 0,5 mol
nKOH dư = nHCl = 0,1 mol
=> nKOH phản ứng = 0,4 mol = nhh axit (1)
=> Mhh = \(\dfrac{22,6}{0,4}\) = 56,5 g/mol
<=> có một axit có M < 56,5 là HCOOH
Giả sử số mol của HCOOH là 3x mol
=> số mol của axit X còn lại là 5x mol
Theo (1) ta có 5x + 3x = 0,4 <=> x = 0,05 mol
=> mHCOOH = 0,05.3.46 = 6,9 gam
<=> m X = 22,6 -6,9 = 15,7 gam
<=> MX = \(\dfrac{15,7}{0,25}\)= 62,8 g/mol (vô lý)
Vậy số mol của HCOOH là 5x = 0,25 mol và số mol của X là 0,15 mol
<=> mX = 22,6 - 0,25.46 = 11,1 g
=> mHCOOH > mX
=> %mHCOOH = \(\dfrac{0,25.46}{22,6}\).100% = 50,88%

a, \(\left\{{}\begin{matrix}n_{Ba^{2+}}=4.10^{-3}\left(mol\right)\\n_{Na^+}=3.10^{-3}\left(mol\right)\\n_{OH^-}=0,011\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left[Ba^{2+}\right]=\dfrac{4.10^{-3}}{0,2+0,3}=0,008M\\\left[Na^+\right]=\dfrac{3.10^{-3}}{0,2+0,3}=0,006M\\\left[OH^-\right]=\dfrac{0,011}{0,2+0,3}=0,022M\end{matrix}\right.\)
b, Để trung hòa dung dịch A thì:
\(n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow0,01.V_{ddHCl}=\left(0,02.2+0,01\right).0,2\)
\(\Leftrightarrow V_{ddHCl}=1\left(l\right)\)

Câu 1:
- Trong NaOH:
pH=14+lg[OH-]\(\rightarrow\)12=14+lg[OH-]\(\rightarrow\)lg[OH-]=-2\(\rightarrow\)[OH-]=10-2=0,01M=[NaOH]
- Trong HCl:
pH=-lg[H+]\(\rightarrow\)1=-lg[H+]\(\rightarrow\)[H+]=10-1=0,1M=[HCl]
\(\rightarrow\)nHCl=0,1.0,01=0,001 mol
NaOH+HCl\(\rightarrow\)NaCl+H2O
nNaOH=nHCl=0,001 mol
\(V_{NaOH}=\dfrac{n}{C_M}=\dfrac{0,001}{0,01}=0,1l=100ml\)
Đáp án C
Câu 2:
HCl+NaOH\(\rightarrow\)NaCl+H2O(1)
nHCl=nNaOH=0,1 mol
HCl+NaAlO2+H2O\(\rightarrow\)NaCl+Al(OH)3(2)
- Trường hợp 1: HCl thiếu so với NaAlO2
\(n_{HCl}=n_{Al\left(OH\right)_3}=0,08mol\)
Suy ra nHCl=0,1+0,08=0,18mol( nếu là trắc nghiệm thì đến đây có thể chọn đáp án C được rồi vì chỉ có đáp án này có 0,18 mol)
- Trường hợp 2: HCl hòa tan hết NaAlO2 và hòa tan 1 phần kết tủa Al(OH)3:
3HCl+Al(OH)3\(\rightarrow\)AlCl3+3H2O(3)
nHCl(pu2)=nAl(OH)3=nNaAlO2=0,1 mol
nHCl(pu3)=3nAl(OH)3(pu3)=3(0,1-0,08)=0,06 mol
Vậy nHCl=0,1+0,1+0,06=0,26 mol
Đáp án C

a, \(n_{H^+}=n_{OH^-}=9.10^{-3}\left(mol\right)\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{\dfrac{9.10^{-3}}{2}}{0,05}=0,09M\)
b, \(\left[SO_4^{2-}\right]=\dfrac{4,5.10^{-3}}{0,05+0,15}=0,6M\)
\(\left[Na^+\right]=\dfrac{0,15.0,06}{0,05+0,15}=0,045M\)
\(\left[H^+\right]=\left[OH^-\right]=\dfrac{9.10^{-3}}{0,05+0,15}=0,045M\)

Gọi thể tích dd A là V(lít)
=> nHCl=0,4V mol, nH2SO4= 0,3V mol
=>\(\sum_{H^+}=\)0,4V+0,3V*2=1*V=V(mol)
DD B có nNaOH=2*0,2=0,4mol, nBa(OH)2=0,5*0,2=0,1mol
=>\(\sum_{OH^-}=\)0,4+0,1*2=0,6 mol
Pứ trung hòa:
__H+ + _OH- → H2O
___0,6<--0,6 (mol)
Mà nH+ =V => V=0,6 lít
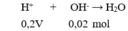
\(C_1\cdot V_1=C_2\cdot V_2\Leftrightarrow C_1\cdot2=0,15\cdot3\Rightarrow0,225l\)