
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: Fe + H2SO4 → FeSO4 + H2↑
Số mol của Fe là: 5,6 : 56 = 0,1 (mol)
Số mol của khí hiđrô là: 0,1 . 1 = 0,1 (mol)
Thể tích Hiđrô thoát ra là: 0,1 . 22,4 = 2,24 (lít)
Số mol của FeSO4 là: 0,1 . 1 = 0,1 (mol)
Khối lượng của chất tan FeSO4 là:
0,1 . 152 = 15,2 (gam)
Số mol H2SO4 là: 0,1 . 1 = 0,1 (mol)
Khối lượng chất tan H2SO4 là:
0,1 . 98 = 9,8 (gam)
Nồng độ phần trăm của dung dịch axit là:
C% = Khối lượng chất tan / Khối lượng dung dịch
=> Khối lượng dung dịch axit là: 9,8 : 40% = 24,5(gam)
Tiếp theo áp dụng định luật bảo toàn khối lượng để tính khối lượng dung dịch sau phản ứng bằng cách cộng tất cả các chất phản ứng trừ đi khối lượng khí.
=> Ta có thể tính được khối lượng dung dịch sau phản ứng = 29,9 gam
C% của dung dịch sau phản ứng là:
( 9,8 : 29,9 ) . 100% = 32,776%

a, \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
b,\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Na_2CO_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{CO_2}=n_{Na_2CO_3}=0,2\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)

a) PTHH : \(Fe+2HCl-->FeCl_2+H_2\)
b) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PTHH : nH2 = nFe = 0,1 (mol)
=> VH2 = \(0,1.22,4=2,24\left(l\right)\)
c) Theo PTHH : \(n_{HCl\left(pu\right)}=2n_{Fe}=0,2\left(mol\right)\)
=> mHCl = 0,2.36,5 = 7,3 (g)

\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
100ml = 0,1l
\(n_{HCl}=3.0,1=0,3\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,3 0,1 0,1
a) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\)
⇒ Mg phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Mg
\(n_{H2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
b) \(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(n_{HCl\left(dư\right)}=0,3-\left(0,1.2\right)=0,1\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
\(C_{M_{HCl\left(dư\right)}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
Chúc bạn học tốt

\(n_{CuSO_4}=0,1.1=0,1\left(mol\right)\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: Fe + CuSO4 --> FeSO4 + Cu
Xét tỉ lệ \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\) => CuSO4 hết, Fe dư
PTHH: Fe + CuSO4 --> FeSO4 + Cu
_____0,1<---0,1---------->0,1
Fe + 2HCl --> FeCl2 + H2
0,05------------------->0,05
=> VH2 = 0,05.22,4 = 1,12(l)
b) \(C_{M\left(FeSO_4\right)}=\dfrac{0,1}{0,1}=1M\)

Để giải bài toán này, ta cần biết phương trình phản ứng giữa Fe và HCl: Fe + 2HCl -> FeCl2 + H2 a. Để xác định nồng độ dung dịch HCl cần dùng, ta cần tính số mol của Fe. Đầu tiên, ta cần chuyển khối lượng Fe thành số mol bằng cách sử dụng khối lượng mol của Fe (56g/mol): Số mol Fe = khối lượng Fe / khối lượng mol Fe = 5,6g / 56g/mol = 0,1 mol Vì theo phương trình phản ứng, 1 mol Fe tương ứng với 2 mol HCl, nên số mol HCl cần dùng là gấp đôi số mol Fe: Số mol HCl = 2 x số mol Fe = 2 x 0,1 mol = 0,2 mol Để tính nồng độ dung dịch HCl, ta chia số mol HCl cho thể tích dung dịch HCl: Nồng độ HCl = số mol HCl / thể tích dung dịch HCl = 0,2 mol / 0,1 L = 2 mol/L Vậy, nồng độ dung dịch HCl cần dùng là 2 mol/L. b. Để xác định khối lượng muối thu được sau phản ứng, ta cần tính số mol muối FeCl2. Theo phương trình phản ứng, 1 mol Fe tương ứng với 1 mol FeCl2, nên số mol muối FeCl2 cũng là 0,1 mol. Khối lượng muối FeCl2 = số mol muối FeCl2 x khối lượng mol muối FeCl2 = 0,1 mol x (56g/mol + 2 x 35,5g/mol) = 0,1 mol x 127g/mol = 12,7g Vậy, khối lượng muối thu được sau phản ứng là 12,7g. c. Để xác định thể tích Hidro thu được sau phản ứng, ta cần tính số mol H2. Theo phương trình phản ứng, 1 mol Fe tương ứng với 1 mol H2, nên số mol H2 cũng là 0,1 mol. Thể tích H2 = số mol H2 x thể tích mol của H2 = 0,1 mol x 22,4 L/mol = 2,24 L Vậy, thể tích Hidro thu được sau phản ứng là 2,24 L.

Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
a. PTHH: Cu + HCl ---x--->
Fe + 2HCl ---> FeCl2 + H2
b. Ta có Cu không phản ứng nên chất rắn sau phản ứng là Cu
=> A = mCu = 6,4(g)
Theo PT: \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(V=V_{H_2}=0,1.22,4=2,24\left(lít\right)\)
c. Hình như thiếu đề nhé.

a) $n_{Fe} = \dfrac{11,2}{56} = 0,2(mol) ; n_{HCl} = \dfrac{300.3,65\%}{36,5} = 0,3(mol)$
$Fe + 2HCl \to FeCl_2 + H_2$
Ta thấy :
$n_{Fe} :1 > n_{HCl} : 2$ nên Fe dư
$n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,15(mol)$
$V_{H_2} = 0,15.22,4 = 3,36(lít)$
b) $n_{FeCl_2} = \dfrac{1}{2}n_{HCl} = 0,15(mol)$
$FeCl_2 + 2NaOH \to Fe(OH)_2 + 2NaCl$
$4Fe(OH)_2 +O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4H_2O$
$n_{Fe_2O_3} = \dfrac{1}{2}n_{FeCl_2} = 0,075(mol)$
$m = 0,075.160 = 12(gam)$

Theo bài ra, ta có: \(m_{Cu}=6,4\left(g\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{12-6,4}{56}=0,1\left(mol\right)=n_{H_2}\)
\(\Rightarrow V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\)
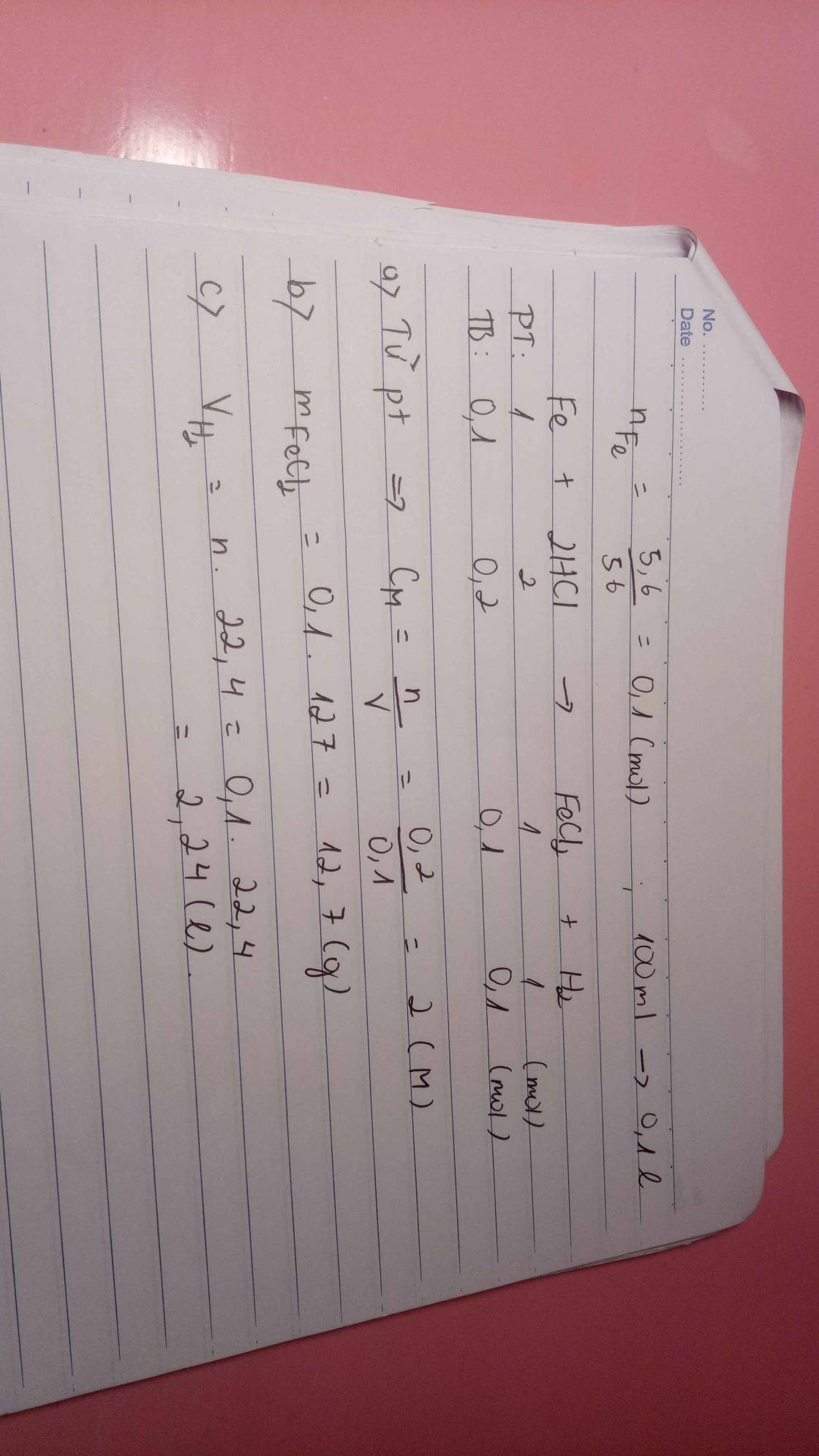
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{Fe}=0,1mol\\ V_{H_2,đktc}=0,1.22,4=2,24l\\ V_{H_2,đkc}=0,1.24,79=2,479l\)