Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức hoá học của hợp chất là: \(Cu_xS_yO_z\)
Ta có: \(64x:32y:16z=40:20:40\)
\(\Rightarrow x:y:z=\dfrac{40}{64}:\dfrac{20}{32}:\dfrac{40}{16}\)
\(\Rightarrow x:y:z=1:1:4\)
Vậy công thức hoá học đơn giản của hợp chất B là: \(\left(CuSO_4\right)n\)
Ta lại có: \(\left(CuSO_4\right)n=160\)
\(\Rightarrow160n=160\)
\(\Rightarrow n=1\)
Vậy công thức hoá học của hợp chất B là:\(CuSO_4\)

Ta có: \(m_{gi\text{ả}m}=m_{CO_2}=3,8\left(g\right)\)
=> \(n_{CO_2}=\dfrac{m}{M}=\dfrac{3,8}{44}=\dfrac{19}{220}\left(mol\right)\)
PTHH: \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=\dfrac{19}{220}\left(mol\right)\)
=> \(m_{CaCO_3}=n.M=\dfrac{19}{220}.100=\dfrac{95}{11}\approx8,64\left(g\right)\)

a)
Ta có: NTK O = 16 đvC
Theo đề ta được:
\(\dfrac{M_O}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow\dfrac{16}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow M_{Zn}=65,38\)

\(Đặt.CTTQ:Cu_aS_mO_z\left(a,m,z:nguyên,dương\right)\\ m_{Cu}=40\%.160=64\left(g\right)\Rightarrow a=n_{Cu}=\dfrac{64}{64}=1\left(mol\right)\\ m_S=20\%.160=32\left(g\right)\Rightarrow m=n_S=\dfrac{32}{32}=1\left(mol\right)\\ m_O=40\%.160=64\left(g\right)\Rightarrow z=n_O=\dfrac{64}{16}=4\\ \Rightarrow a=1;m=1;z=4\\ \Rightarrow CTHH:CuSO_4\)

\(m_{Cu}=\dfrac{80.80}{100}=64g\\ m_O=80-64=16g\\ n_{Cu}=\dfrac{64}{64}=1mol\\ n_O=\dfrac{16}{16}=1mol\\ CTHH:CuO\)

Ta có:
\(M_Y=64\left(\dfrac{g}{mol}\right)\\ \%S=50\%\\ m_S=64.50\%=32\left(g\right)\\ m_O=64-32=32\left(g\right)\\ n_S=\dfrac{32}{32}=1\left(mol\right)\\ n_{O_2}=\dfrac{32}{16}=2\left(mol\right)\\ CTHH:SO_2\)

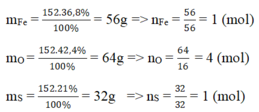
Vậy trong 1 phân tử hợp chất có 1 nguyên tử Fe, 4 nguyên tử O, 1 nguyên tử S.
⇒ CTHH là FeSO4.

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

\(a.\)
\(m_{hh}=0.12\cdot90+0.15\cdot58=19.5\left(g\right)\)
\(b.\)
\(V_{hh}=\left(0.25+0.1+0.05\right)\cdot22.4=8.96\left(l\right)\)
\(c.\)
\(n_A=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(M_A=23\cdot2=46\left(\dfrac{g}{mol}\right)\)
\(m_A=0.45\cdot46=20.7\left(g\right)\)
\(d.\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
Vì CO2 : O2 = 2 : 1
\(\Rightarrow n_{CO_2}=0.2\left(mol\right),n_{O_2}=0.1\left(mol\right)\)
\(m_{hh}=0.2\cdot44+0.1\cdot32=12\left(g\right)\)
\(\overline{M}=\dfrac{12}{0.3}=40\left(\dfrac{g}{mol}\right)\)

hỏi bài kiểu gì
\(M=\dfrac{m}{n}=\dfrac{20}{0,25}=80\left(g/mol\right)\)