Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Áp dụng ĐLBTKL:
mhh = mX + mY + mCO3 = 10 g; mA = mX + mY + mCl = 10 - mCO3 + mCl.
số mol CO3 = số mol CO2 = 0,03 mol.
Số mol Cl = 2 (số mol Cl2 = số mol CO3) (vì muối X2CO3 tạo ra XCl2, Y2CO3 tạo ra 2YCl3).
Do đó: mA = 10 - 60.0,03 + 71.0,03 = 10,33g.

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O

n CO =a
n CO2=b
a+b=0,2
28a +44b=8
=>a=0,05
b=0,15
FexOy +yCO-to->xFe +yCO2
0,15/y <= 0,15
8=(56x +16y).0,15/y
=> x/y=2/3
=> Fe2O3
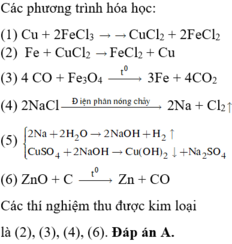
Ý đúng là (2); (3); (4) và (6)
ĐÁP ÁN A