Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Ta có : C = 12 đvC = 1,9926.10-23 (g)
=> 1 đvC = (1,9926.10-23) : 12 ≈ 1,66.10-24 (g).
b. Khối lượng tính bằng gam của nguyên tử nhôm là :
mAl = 27 đvC = 27. 1,66.10-24 = 4,482.10-23 (g)

1 nguyên tử C có khối lượng là:
\(\dfrac{1,9926.10^{-23}}{12}=1,6605.10^{-24}\left(g\right)\)
\(\Rightarrow m_{Ca}=1,6605.10^{-24}.40=6,642.10^{-23}\left(g\right)\)

\(m_{1\text{đ}vC}=\frac{1}{12}\times m_C=\frac{1}{12}\times1,9926\times10^{-23}g=0,166\times10^{-23}g\)
\(m_{gam}\left(P\right)=m_{1\text{đ}vC}\times NTK\left(P\right)=0,166\times10^{-23}g\times31\approx5,15\times10^{-23}g\)
nguyên tử khối của photpho là 31 (1)
khối lượng tính bằng gam của 1 đơn vị cacbon là :
(1,9926 * 10-23) : 12 = 1,66 * 10-24(g)
=> khối lượng tính bằng gam của nguyên tử phốt pho
là : 1,66 * 10-24 * 31 = 5,1*10-23 (g)

a) Ta có khối lượng 1 nguyên tử C = 1,9926 . 10-23 g và bằng 12 đvC
⇒ khối lượng của 1 đơn vị cacbon là
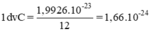
b) Khối lượng tính bằng gam của nguyên tử nhôm
Nhân số trị nguyên tử khối của nhôm với số gam tương ứng của một đơn vị cacbon
MAl = 27x 1,66.10-24 g = 44,82.10-24 g = 4,482.10-23 g.
Đáp án C.

\(1dvC=\dfrac{1}{12}.m_C=\dfrac{1,9926.10^{-23}}{12}=0,16605.10^{-23}\left(g\right)\)
\(NTK_{Cu}=64dvC=64.0,16605.10^{-23}=10,6272.10^{-23}\left(g\right)\)

Biết nguyên tử cacbon có khối lượng bằng 1,9926.10-23 gam. Khối lượng tính bằng gam của nguyên tử Mg bằng bao nhiêu?

a) Ta có : C = 12 đvC = 1,9926.10-23 (g)
=> 1 đvC = ≈ 1,66.10-24 (g).
b) Khối lượng tính bằng gam của nguyên tử nhôm là :
mAl = 27 đvC = 27. 1,66.10-24 = 4,482.10-23 (g)
Đáp án C.
a) Ta có :
\(\Rightarrow\) 1 đvC tương ứng = \(\frac{1,9926.10^{-23}}{12}\)= \(1,6605.10^{-24}\) g
b) Ta có : Al = 27 đvC
\(\Rightarrow\) \(m_{Al}\) = 27. \(1,6605.10^{-24}\) = \(4,482.10^{-23}\) g
Đáp án là C
\(m_{1đ.v.C}=\dfrac{1,9926.10^{-23}}{12}=0,16605.10^{-23}\left(g\right)\\ m_S=32.0,16605.10^{-23}=5,3136.10^{-23}\left(g\right)\)