Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nH2=0,6mol
PTHH: 2Al+6HCl=>2AlCl3+3H2
0,4<-1,2<--0,4 <- 0,6
=> mAl=0,4.27=10,8g
=> m AL2O3=21-10,8=10,2g
=> nAl2O3=0,1mol
PTHH: Al2O3+6HCl=> 2AlCl3+3H2O
0,1--->0,6------>0,2----->0,3
PTHH: AlCl3+3NaOH=> Al(OH)3+3NaCl
nAl(OH)3=0,4mol
nAlCl3=0,4+0,2=0,6mol
ta có : 0,6 : 0,4
=> n AlCl3 dư theo n nAl(OH)3
p/ư: 0,4<-1,2<------0,4--->1,2
=> V (NaOH) cần dùng là : V=1,2:0,5=2,4l

Đáp án:
8,625 g
Giải thích các bước giải:
nCl2=22,4/22,4=1 mol
nNaOH=0,1x2=0,2 mol
nCa(OH)2=0,1x0,5=0,05 mol
2NaOH+Cl2->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2+2Cl2->CaCl2+Ca(ClO)2+2H2O
0,05 0,05 0,025
m=0,025x111+0,1x58,5=8,625 g

a)nAgNO3 = 200 x 8,5 / 100 x 170 = 0,1 mol.
Phương trình hóa học của phản ứng:
HCl + AgNO3 AgCl + HNO3
nHCl = 0,1 mol.
CM(HCl) = 0,1 / 0,15 = 0,67 mol/l.
b) nCo2 = 2,24 /22,4 = 0,1 mol.
Phương trình hóa học của phản ứng:
HCl + NaHCO3 \(\rightarrow\) NaCl + CO2 + H2O.
nHCl = 0,1 mol.
C%HCl = 36,5 x 0,1 /50 x 100% = 7,3%.
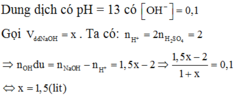
Đáp án B