Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Phản ứng đốt cháy lưu huỳnh:
S + O2 → (t0) SO2
- Khí SO2 sinh ra đã làm chuột chết vì SO2 là khí độc, khi hít phải không khí có SO2 sẽ gây hại cho sức khỏe (gây viêm phổi, mắt, da…), nồng độ cao gây ra bệnh tật thậm chí tử vong.

2. Phản ứng xảy ra khi đốt lưu huỳnh:
S + O2 \(\rightarrow\) SO2
Chất làm chuột chết là khí SO2.
Thể tích nhà kho: V = 6 x 160 = 960 (m3)
Khối lượng lưu huỳnh cần đốt là:
960 x 100 = 96000 gam

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia p.ứng là :
nS = 3,2/32 = 0,1 (mol)
Theo phương trình ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VSO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% thể tích của không khí nên thể tích không khí cần là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
a)Phương trình phản ứng hóa học :
\(S+O_2->SO_2\)
b)Số mol lưu huỳnh thangia phản ứng
\(n_s\) =\(\frac{3,2}{32}\) =0,1(mol)
theo phương trình ta có
\(n_{so2}=n_s=n_{o2}\)
Thể tích khí sunfurơ sing ra được ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
tương tự thể tích khí cần dùng ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
Vì khí õi chiếm 20% về thể tích của không khí veentheer tích không khí cầ dùng là
\(V_{kk}=5.v_{o2}=5.2,24=11,2\left(l\right)\)
Chúc bạn học tốt ![]()
![]()

Ta có: d = Mx:Mh2 = 17 => M của X= 34
Bạn thấy là H chưa biết chiếm bao nhiêu phần trăm trong hợp chất nên ta chỉ cần lấy
100%-94,12%=5,88%
mS= 94,12. 34: 100 xấp xỉ 32
=> ns= m:M= 32:32 = 1
mh=5,88. 34 : 100 xấp xỉ 2
=> nH = 2:1 = 2
vậy công thức hóa học là H2S. Chúc bạn học tốt !
khối lượng X trong công thức là:
17.2.94,12% = 32g = S
khối lượng H2 trong công thức là:
17.2.(100%- 94,12%) = 2g
vậy công thức hh là: H2S

a/ PTHH: S + O2 =(nhiệt)==> SO2
b/ nS = 3,2 / 32 = 0,1 mol
=>nO2 = nSO2 = nS = 0,1 mol
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=>Vkhông khí = \(\frac{2,24.100}{20}\) = 11,2 lít

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

+ Câu a là hiện tượng hóa học vì lưu huỳnh được biến đổi thành lưu huỳnh dioxit.
+ Câu b là hiện tượng vật lí vì khi thủy tinh nóng chảy bị biến dạng (do tác dụng của nhiệt) nhưng thủy tinh vẫn không đổi về chất.
+ Câu c là hiện tượng hóa học vì từ canxi cacbonat dưới tác dụng của nhiệt độ biến đổi thành canxi oxit bay hơi.
+ Câu d là hiện tượng vật lí, vì cồn bị bốc hơi ra khỏi lọ do tính chất vật lí chứ không tác dụng với một chất nào khác.
+ Câu a là hiện tượng hóa học vì lưu huỳnh được biến đổi thành lưu huỳnh dioxit.
+ Câu b là hiện tượng vật lí vì khi thủy tinh nóng chảy bị biến dạng (do tác dụng của nhiệt) nhưng thủy tinh vẫn không đổi về chất.
+ Câu c là hiện tượng hóa học vì từ canxi cacbonat dưới tác dụng của nhiệt độ biến đổi thành canxi oxit bay hơi.
+ Câu d là hiện tượng vật lí, vì cồn bị bốc hơi ra khỏi lọ do tính chất vật lí chứ không tác dụng với một chất nào khác.

a) PTHH: S + O2 =(nhiệt)=> SO2
b) nS = 3,2 / 32 = 0,1 (mol)
=> nO2 = nSO2 = nS = 0,1 (mol)
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VKK(đktc) = \(2,24\div\frac{1}{5}=11,2\left(l\right)\)
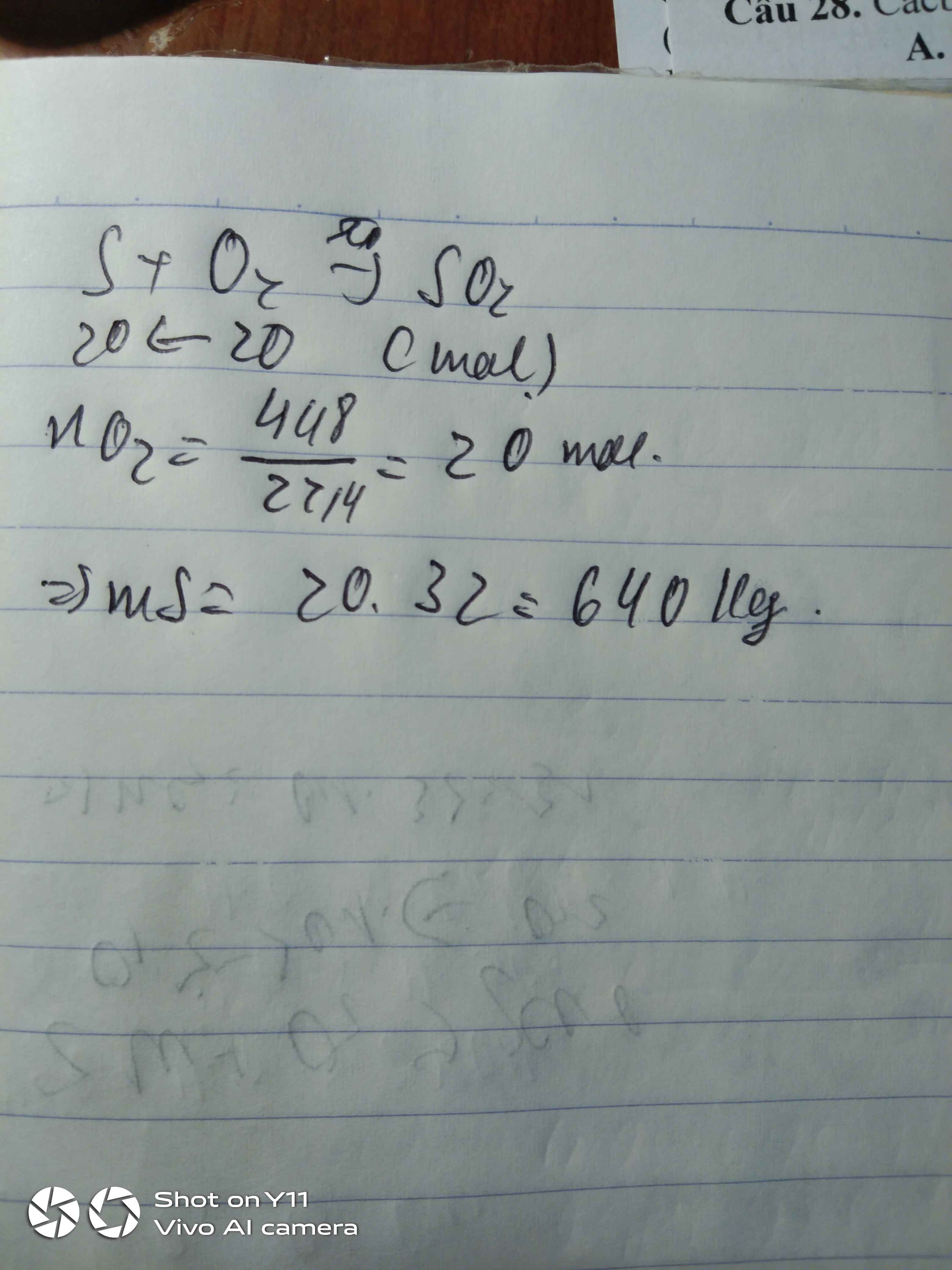
a) PTHH \(S+O_2\underrightarrow{t^o}SO_2\)
b) Khí SO2 chính là chất làm cho chuột chết. Hợp chất này tên là lưu huỳnh đi-ô-xít (tên Tiếng Anh là sulfur dioxide). Đây là một oxit axit.