Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Từ phương trình: \(p_V=nRT\)
Suy ra:
\(V=\frac{nRT}{p}=\frac{3\times8.31\times300}{600000}=0.012\left(m^3\right)=12\left(l\right)\)

Biết ρ 0 = m/ V 0 và ρ = m/V ⇒ ρ 0 V 0 = ρ V
Mặt khác p 0 V 0 = pV
(vì nhiệt độ của khí bằng nhiệt độ ở điều kiện chuẩn).
Từ (1) và (2) suy ra:
ρ = ρ 0 p/ p 0 = 1,43.150/1 = 214,5(kg/ m 3 )
Và m = 214,5. 10 - 2 = 2,145 kg.

V 0 ≈ 1,889 lít. Vì áp suất quá lớn nên khí không thể coi là khí lí tưởng. Do đó kết quả tìm được chỉ là gần đúng.

Xét lượng khí trong bình.
Trạng thái đầu: V 1 = 8 lít; T 1 = 100 + 273 = 373 K ; p 1 = 10 5 N/ m 2
Trạng thái cuối: V 2 = 8 lít; T 2 = 20 + 273 = 293 K; p 2 = ?
Vì thể tích không đổi nên:
p 1 / T 1 = p 2 / T 2 ⇒ p 2 = p 1 T 2 / T 1 = 7,86. 10 4 N/ m 2

Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn: { V 1 = m p = 3 , 96 1 , 98 m 3 = 2 m 3 p 1 = p 0 = 1 a t T 1 = 0 0 C = 273 K
Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ { V 2 = 0 , 04 m 3 p 2 = 60 a t T 2 = ?
Áp dụng công thức
p 1 V 1 T 1 = p 2 V 2 T 2 ⇒ T 2 = p 2 V 2 T 1 p 1 V 1 = 60.0 , 04.273 1.2 T 2 = 327 , 6 K
Mà T 2 = 273 + t 2 = 327 , 6 K ⇒ t 2 = 54 , 6 0 C

+ Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn:
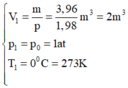
+ Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ:


Chọn A.
Ở điều kiện chuẩn p1 = 760 mmHg; ρ = 1,29 kg/m3.
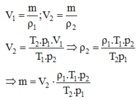
là khối lượng khí bơm vào bình sau nửa giờ.
khối lượng bơm vào sau mỗi giây:
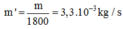

Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic: