Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)2H2O + 5SO2 + 2 KMnO4 ->K2SO4 +2 MnO4 + 2H2SO4
b)SO2 :chất khử
KMnO4 : chất oxi hóa

cho H2SO4 vào đầu tiên nhận biết được Ba(NO3)2 :Ba(NO3)2 +H2SO4 tạo ra BaSO4 kết tủa +HNO3
cho Ba(NO3)2 vào 3 chất còn lại trong phản ứng chất nào sinh ra kết tủa là Na2SO4,sinh ra chất khí là HCL,không có hiện tượng gì là NaCL.
| Chất thử\dd | NaCl | HCl | Na2SO4 | Ba(NO3)2 |
| H2SO4 | x | x | x | \(\downarrow\) trắng |
| BaCl2 | x | x | \(\downarrow\)trắng | |
| Fe | x | \(\uparrow\)H2 |
Ba(NO3)2 + H2SO4 -->BaSO4\(\downarrow\) + 2HNO3
BaCl2 + Na2SO4 -->BaSO4\(\downarrow\) + 2NaCl
Fe + 2HCl --> FeCl2 + H2\(\uparrow\)

em mới học lớp 9 thôi nhưng theo em thì:
vai trò: do c2h2 không tác dụng trực tiếp với agno3. Nên phải dùng đến xúc tác NH3
dùng Nh3 do có tính khử kèm tính 3 dơ yếu
Nh3+h2o-->Nh4Oh

Có thể xem công thức Fe3O4 là FeO.Fe2O3 nên hỗn hợp X có thể được xem như gồm FeO và Fe2O3.
Gọi a là số mol FeO, b là số mol Fe2O3 của 0,5 m gam X.
FeO + H2SO4 --->FeSO4 + H2O
Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 + 3H2O
từ khối lượng muối khan ở phần 1, ta có phương trình
152a + 400b = 31,6 gam (1)
Phần 2 khi cho Cl2 vào thì xảy ra pu:
FeSO4 + 0,5 Cl2 ---> 1/3 Fe2(SO4)3 + 1/3 FeCl3
--> khối lượng muối ở phần 2 = 400a/3 + 162,5a/3 + 400b = 33,375 gam
--> 562a + 1200b = 100,125 (2)
Từ (1) và (2) suy ra :
a =0,0502358 mol
b = 0,0599153 mol
--> Khối lượng hỗn hợp X = 2 x (72 x 0,0502358 + 160 x 0,0599153) = 26,712448 gam
a.
Phương trình
+ Khi hòa A bằng axit H2SO4 loãng
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O (1)
Fe2O3 + 3H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3H2O (2)
Fe3O4 + 4H2SO4 \(\rightarrow\) Fe2(SO4)3 + FeSO4+ 3H2O (3)
Sau phản ứng dung dịch chỉ có 2 muối (x+z)mol FeSO4 và (y+z) mol Fe2(SO4)3
+ Khi sục khí Cl2 vào dung dịch sau phản ứng chỉ có FeSO4 phản ứng
6FeSO4 + 3Cl2 \(\rightarrow\) 2FeCl3 + 2Fe2(SO4)3 (4)
b.
Theo bài ta có hệ phương trình
\(\begin{cases}72x+160y+232z=m\text{/}2\\152\left(x+z\right)+400\left(y+z\right)=31,6\\187,5\left(x+z\right)+400\left(y+z\right)=33,375\end{cases}\)\(\begin{matrix}\left(I\right)\\\left(II\right)\\\left(III\right)\end{matrix}\)
Từ II, III ta có x+z= 0,05; y+z=0,06
Mặt khác từ I ta có m=2.[ 72(x+z) + 160(y+z)]=26,4 gam
Vậy m= 26,4g
\(C_{FeSO_4}\)=0,2M; \(C_{Fe_2\left(SO_4\right)_3}\)=0,24M

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = = CM(NaClO) =
= 1,6 mol/l
CM(NaOH)dư = = 0,8 mol/l

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = = CM(NaClO) =
= 1,6 mol/l
CM(NaOH)dư = = 0,8 mol/l
500 ml = 0,5l
\(n_{NaOH}=0,5.4=2\left(mol\right)\)
\(n_{MnO_2}=\frac{69,6}{87}=0,8\left(mol\right)\)
a, \(MnO_2+4HCl->MnCl_2+Cl_2+2H_2O\) (1)
\(Cl_2+2NaOH->NaCl+NaClO+H_2O\) (2)
theo (1) \(n_{Cl_2}=n_{MnO_2}=0,8\left(mol\right)\)
vì \(\frac{0,8}{1}< \frac{2}{2}\) => NaOH dư
theo (2) \(n_{NaOH\left(pư\right)}=2n_{Cl_2}=1,6\left(mol\right)\)
=> \(n_{NaOH\left(dư\right)}=2-1,6=0,4\left(mol\right)\)
theo (2) \(n_{NaCl}=n_{Cl_2}=0,8\left(mol\right)\)
nồng độ mol của các chất trọng dung dịch sau phản ứng là
\(C_{M\left(NaCl\right)}=\frac{0,8}{0,5}=1,6M\)
\(C_{M\left(NaOH\right)dư}=\frac{0,4}{0,5}=0,8\left(mol\right)\)
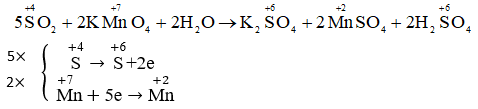
nêu hiện tượng, viết phương trình phản và nêu vai trò của các chất tham gia phản ứng khi dẫn khí SO2 lần lượt vào:
dung dịch brom có màu vàng nâu nhạt
SO2+ Br2 +2H2O->H2SO4+2HBr
chất khử....chất oxi hoá
dung dịch axit sunfuhidric
SO2+ 2H2S->2H2O+3S
chất oxi hoá-- chất khử
dung dịch KMnO4