Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\) \(n_{H_2SO_4}=0,3.0,25=0,075\left(mol\right)\)
\(X+H_2SO_{4\left(l\right)}\rightarrow XSO_4+H_2\uparrow\)
0,06 0,06 0,06 0,06 (mol)
dư:0 0,015 0 0 (mol)
b/
m\(M_X=\dfrac{3,36}{0,06}=56\left(g\right)\)
\(\rightarrow Fe\)
c/
\(2Fe+6H_2SO_{4\left(đn\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,06 0,09 (mol)
V\(_{SO_2}=0,09.22,4=2,016\left(l\right)\)

1.
2M + 2xHCl \(\rightarrow\)2MClx + xH2
nH2=\(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PTHH ta có:
nM=\(\dfrac{2}{x}\)nH2=\(\dfrac{0,6}{x}\)
MM=\(\dfrac{5,4}{\dfrac{0,6}{x}}=9x\)
Với x=3 thì MM=27
Vậy M là Al

\(Mg\left(x\right)+2HCl\rightarrow MgCl_2+H_2\left(x\right)\)
\(2Al\left(y\right)+6HCl\rightarrow2AlCl_3+3H_2\left(1,5y\right)\)
\(Fe\left(z\right)+2HCl\rightarrow FeCl_2+H_2\left(z\right)\)
\(Mg\left(x\right)+Cl_2\left(x\right)\rightarrow MgCl_2\)
\(2Al\left(y\right)+3Cl_2\left(1,5y\right)\rightarrow2AlCl_3\)
\(2Fe\left(z\right)+3Cl_2\left(1,5z\right)\rightarrow2FeCl_3\)
Gọi số mol của Mg, Al, Fe trong hỗn hợp lần lược là x, y, z ta có
\(24x+27y+56z=26,05\left(1\right)\)
Số mol H2: \(\frac{13,44}{22,4}=0,6\)
\(\Rightarrow x+1,5y+z=0,6\left(2\right)\)
Số mol Cl2 là: \(\frac{17,36}{22,4}=0,775\)
\(\Rightarrow x+1,5y+1,5z=0,775\left(3\right)\)
Từ (1), (2), (3) ta có hệ: \(\left\{\begin{matrix}24x+27y+56z=26,05\\x+1,5y+z=0,6\\x+1,5y+1,5z=0,775\end{matrix}\right.\)
M ra đáp số âm không biết có phải do đề sai không

Đáp án B
Xét giai đoạn m gam Fe tác dụng với dung dịch H2SO4 loãng:
Sơ đồ phản ứng :
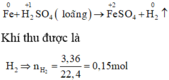
Các quá trình nhường, nhận electron :
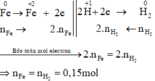
Xét giai đoạn m gam Fe tác dụng với H2SO4 đặc, nóng , dư:
Sơ đồ phản ứng:
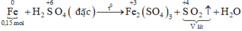
Các quá trình nhường, nhận electron:
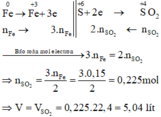

a)
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4 → FeSO4 + H2
b) Gọi số mol Zn và Fe có trong 17,7 gam hỗn hợp là x và y mol. nH2 = \(\dfrac{6,72}{22,4}\)=0,3 mol
Theo tỉ lệ phản ứng ta có\(\left\{{}\begin{matrix}x+y=0,3\\65x+56y=17,7\end{matrix}\right.\)=> x = 0,1 và y = 0,2
=>%n Zn=\(\dfrac{0,1}{0,3}100=33,33\%\)
=>%n Fe=66,67%
=>m muối= 0,1.161+0,2.152=46,5g
Gọi số mol Fe, Zn là a, b (mol)
=> 56a + 65b = 17,7 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----------------->a--->a
Zn + H2SO4 --> ZnSO4 + H2
b------------------->b----->b
=> a + b = 0,3 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%n_{Fe}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%n_{Zn}=\dfrac{0,1}{0,3}.100\%=33,33\%\end{matrix}\right.\)
mmuối = 0,2.152 + 0,1.161 = 46,5 (g)

Gọi \(n_{N_2O} = a ; n_{N_2} = b(mol)\)
Ta có :
\(n_{khí} = a + b = 0,027(mol)\\ m_{khí} = 44a + 28b = M.n = 18,45.2.0,027 = 0,9963(gam)\)
Suy ra a = 0,015 ; b = 0,012
Bảo toàn electron :
\(3n_M = 8n_{N_2O} + 10n_{N_2} = 0,015.8 + 0,012.10 = 0,24\\ \Rightarrow n_M = 0,08(mol)\\ \Rightarrow M = \dfrac{2,16}{0,08} = 27(Al)\)
Vậy kim loại M là Al

\(\text{Fe+H2SO4=FeSO4+H2}\)
Ta có :
\(\text{nH2=1,792/22,4=0,08mol}\)
\(\text{=>nFe=0,08mol}\)
Khi cho 0,08mol Fe td với HNO3:
Quá trình nhường e: Fe=Fe+3 +3e
=> n e nhường=0,24mol
Theo ĐLBTe, ta có n e cho=n e nhận.
Quá trình nhận e: \(\text{N+5 +3e=>N+2}\)
\(\text{=> nN+2=0,24/3=0,08mol}\)
\(\text{=>nNO=0,08mol =>V NO=0,08.22,4=1,792l}\)
Fe+H2SO4--->FeSO4+H2
Fe+4HNO3---->Fe(NO3)3+NO+2H2O
n H2=0,08(mol)
Theo pthh1
n Fe =n H2 =0,08(mol)
m Fe=0,08.56=4,48(g)=m
Theo pthh2
n NO=n Fe=0,08(mol)
V NO= V=0,08.22,4=1,792(l)