Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ta có: \(\left\{{}\begin{matrix}n_{Al}=\dfrac{1,35}{27}=0,05\left(mol\right)\\n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,05}{2}>\dfrac{0,1}{6}\) \(\Rightarrow\) Nhôm dư, tính theo HCl
\(\Rightarrow n_{AlCl_3}=\dfrac{1}{30}\left(mol\right)\) \(\Rightarrow m_{AlCl_3}=\dfrac{1}{30}\cdot133,5=4,45\left(g\right)\)
\(\Rightarrow\) Chọn A
Ta có: \(n_{Al}=\dfrac{1,35}{27}=0,05\left(mol\right)\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\)
\(PTHH:2Al+6HCl--->2AlCl_3+3H_2\)
Ta thấy: \(\dfrac{0,05}{2}>\dfrac{0,1}{6}\)
Vậy Al dư.
Theo PT: \(n_{AlCl_3}=\dfrac{1}{3}.n_{HCl}=\dfrac{1}{3}.0,1=\dfrac{1}{30}\left(mol\right)\)
\(\Rightarrow m_{AlCl_3}=\dfrac{1}{30}.133,5=4,45\left(g\right)\)
Chọn A

Gọi x, y là số mol của 2 chất H2NCH2COONa và H2NCH2CH2COONa
Khối lượng hỗn hợp muối ban đầu:
m(hh muối) = m(H2NCH2COONa) + m(H2NCH2COONa) = 97x + 111y = 25,65gam [1]
Cho dung dịch muối tác dụng với dung dịch H2SO4:
2NaOOCCH2NH2 + 2H2SO4 → (HOOCCH2NH3)2SO4 + Na2SO4
x x
2NaOOCCH2CH2NH2 + 2H2SO4 → (HOOCCH2NH3)2SO4 + Na2SO4
y y
Số mol H2SO4 cần dùng: n(H2SO4) = x + y = 1.0,25 = 0,25mol [2]
Giải hệ PT [1], [2] ta được: x = 0,15mol và y = 0,1mol
Theo ĐL bảo toàn khối lượng, tổng khối lượng muối do H2NCH2COONa tạo thành:
m(hh muối) = m(NaOOCCH2NH2) + 98x = 0,15.97 + 0,15.98 = 29,25 gam
Đáp án A.

nAl2O3= 10,2/102= 0,1(mol)
a) PTHH: Al2O3 + 6 HCl -> 2 AlCl3 + 3 H2O
0,1_______0,6_______0,2_________0,3(mol)
mHCl=0,6.36,5= 21,9(g)
=>mddHCl= (21,9.100)/7,3=300(g)
b) mddsau= mAl2O3 + mddHCl= 10,2+300=310,2(g)
c) mAlCl3= 133,5.0,2=26,7(g)
=>C%ddAlCl3= (26,7/310,2).100=8,607%

1)
a, \(n_{Al}=\dfrac{15,3}{102}=0,15\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,15 0,9 0,3
\(m_{ddHCl}=\dfrac{0,9.36,5.100}{20}=164,25\left(g\right)\)
b, mdd sau pứ = 15,3 + 164,25 = 179,55 (g)
c, \(C\%_{ddAlCl_3}=\dfrac{0,3.133,5.100\%}{179,55}=22,31\%\)
2)
a, \(m_{HCl}=54,75.20\%=10,95\left(g\right)\Rightarrow n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Al_2O_3}=0,05.102=5,1\left(g\right)\)
b, mdd sau pứ = 5,1 + 54,75 = 59,85 (g)
\(C\%_{ddAlCl_3}=\dfrac{0,1.133,5.100\%}{59,85}=22,31\%\)

\(4.\\ a/n_{Al}=\dfrac{5,4}{27}=0,2mol\\2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(0,2......0,3............0,1...............0,3\)
\(V_{H_2}=0,3.24,79=7,437l\\ b.C_{\%H_2SO_4}=\dfrac{0,3.98}{150}\cdot100=19,6\%\\ c.m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2g\)

Kl Oxi: m(O) = [m(0xit) - m(Kim loai)] = (22,3 - 14,3) = 8
====> n(0) = 8/16 = 0,5(m0l)
Theo bảo toàn nguyên tố ta có:
+, n(H20) = n(0) = 0,5 (mol)
+, n(HCl) = 2n(H20) = 0,5*2 = 1 (m0l)
Theo bảo toàn khối lượng:
m(Oxit) + m(Axit) = m(Muối) + m(Nước)
=====> m(Muối) = m(0xit) + m(Axit) - m(H20) = 22,3 + 36,5*1 - 18*0,5 = 49,8

\(4.a/n_{Al}=\dfrac{5,4}{27}=0,2mol\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 0,1 0,3
\(V_{H_2}=0,3.24,79=7,437l\\ b/C_{\%H_2SO_4}=\dfrac{0,3.98}{150}\cdot100=19,6\%\\ c/m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2g\)
\(5.a/n_{MgO}=\dfrac{4}{40}=0,1mol\\ MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,1 0,2 0,1 0,1
\(C_{\%HCl}=\dfrac{0,2.36,5}{200}\cdot100=3,65\%\\ b/C_{\%MgCl_2}=\dfrac{0,1.95}{200+4}\cdot100=4,66\%\\ c/NaOH+HCl\rightarrow NaCl+H_2O\\ n_{NaOH}=n_{HCl}=0,2mol\\ V_{NaOH}=\dfrac{0,2}{1}=0,2l=200ml\)

2Al + 6HCl → 2AlCl3 + 3H2
2 6 2 3
0,3 0,9 0,3 0,45
a). nAl= \(\dfrac{8,1}{27}\)=0,3(mol)
⇒ nHCl= \(\dfrac{0,3.3}{6}\)= 0,9(mol).
⇒ mHCl=n.M= 0,9 . 36.5 =32,85(g).
b). nAlCl3= \(\dfrac{0,9.2}{6}\)= 0,3(mol).
⇒mAlCl3= n.M = 0,3 . 133,5 =40,05(g).
c). nH2= \(\dfrac{0,3.3}{2}\)= 0,45(mol).
⇒VH2= n . 22,4 = 0,45 . 22,4= 10,08(g).
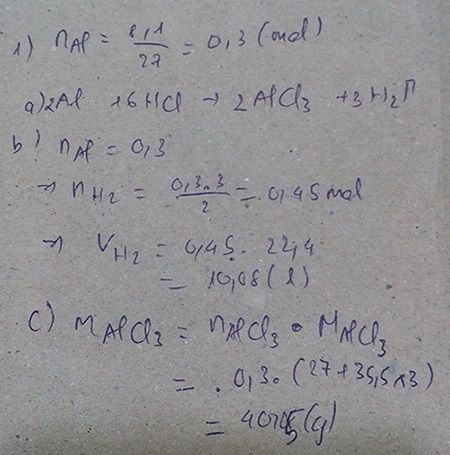
ai còn on ko vậy ????????????
\(n_{Al}=m_{Al}:M_{Al}=1,35:27=0,05mol\)
\(n_{HCl}=m_{HCl}:M_{HCl}=7,3:36,5=0,2mol\)
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Pứ: 0,05 0,2 ?mol
Có: \(\frac{0,05}{2}< \frac{0,2}{6}\)
-> Al phản ứng hết, HCl dư
Từ PTHH: \(n_{AlCl_3}=n_{Al}=0,05mol\)
\(\rightarrow m_{AlCl_3}=n_{AlCl_3}.M_{AlCl_3}=0,05.\left(27+3+35,5\right)=6,675g\)