Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

9
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g) =>D
10
nBa(OH) = 0,15.1 = 0,15mol; nBaCO3 = 19,7 : 197 = 0,1mol
Vì nBaCO3 < nBa(OH)2 → xét 2 trường hợp
Trường hợp 1: Ba(OH)2 dư, CO2 hết, phản ứng chỉ tạo muối cacbonat
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
Vậy V = VCO2 = 0,1.22,4 =2,24
Trường hợp 2: Phản ứng sinh ra 2 muối cacbonat và hiđrocacbonat
CO2 + Ba(OH)2→ BaCO3 + H2O (1)
0,1 0,1 0,1
2CO2+Ba(OH)2→Ba(HCO3)2
0,1 0,05
Theo phương trình (1): nBa(OH)2(1) = nBaCO3=0,1mol
Mà nBa(OH)2= 0,15mol →nBa(OH)2 (2) = 0,15−0,1 = 0,05mol
Theo (1) và (2): nCO2 = nBaCO3 + 2nBa(OH)2 (2) = 0,1 + 2.0,05 = 0,2 mol
Vậy V = VCO2 = 0,2.22,4 = 4,48 lít
=>A

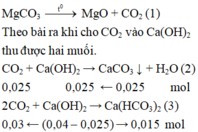
C a H C O 3 2 + 2 N a O H d ư → C a C O 3 ↓ + N a 2 C O 3 + 2 H 2 O ( 4 ) 0 , 015 → 0 , 015 m o l
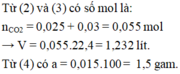
Đáp án A

\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(n_{CaO}=n_{Ca\left(OH\right)_2}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{1,2}{100}=0,012\left(mol\right)\)
TH1: CO2 hết, Ca(OH)2 dư
PTHH: Ca(OH)2 + CO2 -----> CaCO3 + H2O
0,012 -> 0,012 mol
=> VCO2 = 0,012 . 22,4 = 0,27 (l)
TH2: CO2 dư
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
0,06 ..............0,06......0,06
CO2 + CaCO3 + H2O -> Ca(HCO3)2
0,048<--(0,06 - 0,012)
=> nCO2 = 0,06 + 0,048 = 0,108 mol
=> VCO2 = 0,108 . 22,4 = 2,42 (l)

Ca(OH)2+Co2->CaCO3+H2O(1)
Ca(OH)2+2Co2->Ca(HCO3)2
Ca(HCO3)2->CaCO3+CO2+H2O
\(\left(1\right)=>nCO2=nCaCO3=\dfrac{550}{100}=5,5mol\)
\(=>nCO2=5,5+2.\dfrac{100}{100}=7,5mol\)
\(=>VCO2=168l\)

Sửa đề : 500 ml dung dịch Ca(OH)2 0,1M . Nếu là 0,01M thì đề sai
\(n_{Ca\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố Ca : \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}\)
=> \(n_{Ca\left(HCO_3\right)_2}=0,05-0,02=0,03\left(mol\right)\)
Bảo toàn nguyên tố C :
=> \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,02+0,03.2=0,08\left(mol\right)\)
=> \(V_{CO_2}=0,08.22,4=1,792\left(l\right)\)

Chọn A
n C a O = 0 , 1 m o l ; n S O 2 = 0 , 125 m o l
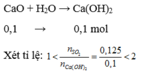
=> phản ứng sinh ra 2 muối CaS O 3 (x mol) và Ca(HS O 3 ) 2 (y mol)


Ta có: \(n_{CO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(m_{NaOH}=160.1\%=1,6\left(g\right)\Rightarrow n_{NaOH}=\dfrac{1,6}{40}=0,04\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{CO_2}}=0,8\)
⇒ Pư tạo muối NaHCO3.
PT: \(CO_2+NaOH\rightarrow NaHCO_3\)
__________0,04_______0,04 (mol)
⇒ mNaHCO3 = 0,04.84 = 3,36 (g)
Bạn tham khảo nhé!
\(n_{CO_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{NaOH}=\dfrac{160\cdot1\%}{40}=0.04\left(mol\right)\)
\(T=\dfrac{0.04}{0.05}=0.8\)
\(\Rightarrow\text{Tạo muối axit}\)
\(NaOH+CO_2\rightarrow NaHCO_3\)
\(0.04.......................0.04\)
\(m_{NaHCO_3}=0.04\cdot84=3.36\left(g\right)\)

\(n_{BaCO_3}=\dfrac{9,85}{197}=0,05\left(mol\right)\)
Cho dd NaOH dư vào vẫn thu được kết tủa `->` trong dd có \(Ba\left(HCO_3\right)_2\)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\)
0,05 0,05 ( mol )
\(n_{BaCO_3}=\dfrac{1,97}{197}=0,01\left(mol\right)\)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
0,02 0,01 ( mol )
\(Ba\left(HCO_3\right)_2+2NaOH\rightarrow BaCO_3\downarrow+Na_2CO_3+2H_2O\)
0,01 0,01 ( mol )
\(n_{CO_2}=0,05+0,02=0,07\left(mol\right)\)
\(V_{CO_2}=0,07.22,4=1,568\left(l\right)\)


45.
\(n_{SO2}=\frac{38,528}{22,4}=1,72\left(mol\right)\)
\(m_{NaOH}=\frac{2832.100}{100}=283,2\left(g\right)\)
\(\Rightarrow n_{NaOH}=283,2:40=7,08\left(mol\right)\)
Tỉ lệ \(\frac{n_{NaOH}}{n_{SO2}}=4,12>2\Rightarrow\) Na2SO3 hết , NaOH dư
\(PTHH:SO_2+NaOH\rightarrow Na_2SO_3+H_2O\)
______1,72______1,72___________________
\(\Rightarrow m_{Na2SO3}=\frac{1,72}{126}=216,72\left(g\right)\)
46.
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,1_______________0,1 _________(mol)
\(n_{Ca\left(OH\right)2}=0,5.0,3=0,15\left(mol\right)\)
\(n_{CaCO3}=\frac{10}{100}=0,1\left(mol\right)\)
Tỉ lệ : \(\frac{0,15}{1}>\frac{0,1}{1}\Rightarrow\) nCa(OH)2 phản ứng dư, nCaCO3 phản ứng hết
\(\Rightarrow V_{CO2}=0,1.22,4=2,24\left(l\right)\)
47.
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(\Rightarrow n_{Ca\left(OH\right)2}=n_{CaO}=0,1\left(mol\right)\)
\(n_{CaSO3}=0,01\left(mol\right)\)
- TH1: Dư kiềm
\(Ca\left(OH\right)_2+SO_2\rightarrow CaSO_3+H_2O\)
\(\Rightarrow n_{SO2}=n_{CaSO3}=0,01\left(mol\right)\)
\(\Rightarrow V=0,01.22,4=0,224\left(l\right)\)
- TH2: Dư SO2
\(Ca\left(OH\right)_2+SO_2\rightarrow CaSO_3+H_2O\)
\(\Rightarrow n_{SO2_{kt}}=n_{Ca\left(OH\right)2}=n_{CaSO3}=0,1\left(mol\right)\)
Vậy Có 0,1- 0,01 = 0,09 mol CaSO3 tan
\(CaSO_3+SO_2+H_2O\rightarrow Ca\left(HSO_3\right)_2\)
\(\Rightarrow n_{SO2_{kt}}=0,09\left(mol\right)\)
Tổng mol SO2= 0,19 mol
\(\Rightarrow V=0,19.22,4=4,256\left(l\right)\)
48.
\(n_{NaOH}=0,781\left(mol\right)\)
Gọi a là mol NaHSO3, b là mol Na2SO3
\(\Rightarrow104a+126b=79,338\left(1\right)\)
\(NaOH+SO_2\rightarrow NaHSO_3\)
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(\Rightarrow a+2b=0,781\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=0,735\\b=0,023\end{matrix}\right.\)
\(m_{NaHSO3}=104.0,735=76,44\left(g\right)\)
\(m_{Na2SO3}=126.0,023=2,898\left(g\right)\)
ai trả lời giúp mình vs mình đg cần gấp