Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\({\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 1} {\rm{H = O + }}{\mathop {{\rm{Br}}}\limits^0 _{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 3} {\rm{OOH + 2H}}\mathop {{\rm{Br}}}\limits^{ - 1} \)
Trong phản ứng trên, số oxi hoá của C (trong nhóm chức –CHO) tăng từ +1 lên +3, CH3CHO là chất oxi hóa. Số oxi hóa của Br giảm từ 0 xuống -1 , Br2 là chất oxi hóa.

CH4+ Cl2 → CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl

Trong phản ứng này: I2 đóng vai trò là chất oxi hoá (do số oxi hoá giảm từ 0 xuống -1 sau phản ứng); NaOH đóng vai trò là môi trường phản ứng (do số oxi hoá không thay đổi sau phản ứng).

Phương trình điều chế hiđro
CH4 + 2H2O -to, xt→ CO2 + 4H2
Phương trình loại khí oxi:
CH4 + 2O2 -to→ CO2 + 2H2O
Phương trình tống hợp amoniac:
N2 + 3H2 -450-500o, Fe, 200-300atm→ 2NH3

Tham khảo:
Alkyne có nguyên tử hydrogen linh động, phân tử chứa 4 nguyên tử Carbon là CH≡C−CH2−CH3
PTHH:
CH≡C−CH2−CH3 + [Ag(NH3)2]OH → CAg≡C−CH2−CH3 + NH4NO3
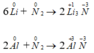
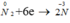
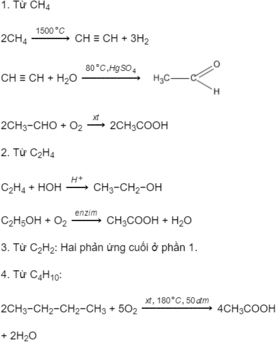
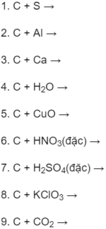



2.
\(\dfrac{1}{2}N_2+\dfrac{3}{2}H_2-t^0->NH_3\)
N có số oxy hoá thay đổi từ 0 sang -3; H có số oxy hoá từ 0 sang +1.
3.
N2(g) + O2(g) ⇌ 2NO(g)
a. N có số oxy hoá thay đổi từ 0 sang +2; O có số oxy hoá từ 0 sang -2.
b. Vì đây là phản ứng cần năng lượng cao mà hiệu suất kém, đi kèm với lãng phí, tiêu hao nhiên liệu.