Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

a) Nhận xét: 33,84g X > 16g rắn → kim loại còn dư.
Chú ý: sau một thời gian ám chỉ các chất tham gia đều dư.
Giả sử số mol của Mg, Fe lần lượt là x, y
Tăng giảm khối lượng: (64 – 24) . x + (64 – 56) . y = 38,24 – 33,84 (1)
Chất rắn bao gồm MgO: x; Fe2O3: 0,5y; CuO: a – x – y
=> 40x + 160 . 0,5y + 80(a – x – y) = 16 (2)
Từ (1) và (2) => 10a + y = 2,55
amax <=> y = 0 => amax = 0,255
b) giá trị a đạt max thì Fe chưa tham gia pứ.
Giả sử số mol Mg dư là: z (mol) 19,12g Z cho 0,48 mol SO2 → 38,24g Z cho 0,96 mol SO2
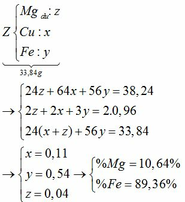

2Al+6HCl---->2AlCl3+3H2
Al2o3+6HCl--->2AlCl3+3H2O
Cu+HCl--> không p/u
2Cu + O2---->2CuO
ncuO=2,75/80=0.034375(mol)
Cứ 2 mol Cu---à 2 mol CuO
0.034375<------0.034375
mCu=0,034375.64=2,2(g)
--->%mCu=2,2.100/10=22%
nH2=3,36/22,4=0,15(mol)
cứ 2 mol Al----->3 mol H2
0.1<-----0.15
mAl :0,1.27=2.7(g)
--->%mAl=2,7.100/10=27%
---->%mAl2o3=100%-27%-22%=51%

a)
$2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
Gọi $n_{CuO} = n_{Cu(NO_3)_2\ pư} = a(mol)$
Suy ra:
$m_{giảm} = 188a - 80a = 54 \Rightarrow a = 0,5(mol)$
$m_{Cu(NO_3)_2\ pư} = 0,5.188 = 94(gam)$
b)
$n_{NO_2} = 4a = 2(mol)$
$n_{O_2} = 0,5a = 0,25(mol)$
$V_{NO_2} = 2.22,4 = 44,8(lít)$
$V_{O_2} = 0,25.22,4 = 5,6(lít)$
Bài 1 :
PTHH : 2Cu(NO3)2 -> 2CuO + 4NO2 \(\uparrow\) + O2 \(\uparrow\)
............. \(\dfrac{m}{250}\)................................\(\dfrac{m}{125}\).......\(\dfrac{m}{500}\) (mol)
Gọi khối lượng Cu(NO3)2 đem đi nhiệt phân là m (g)
Theo bài ra ta có hệ :
\(m-m_{NO2\uparrow}-m_{O2\uparrow}=m-0,54\left(g\right)\)
<=> m - \(\left(\dfrac{46m}{125}+\dfrac{32m}{500}\right)=m-0,54\)
<=> \(\dfrac{46m}{125}+\dfrac{32m}{500}=0,54\left(g\right)\)
<=> \(\dfrac{54m}{125}=0,54\left(g\right)\Rightarrow m=1,25\left(g\right)\)
Vậy khối lượng Cu(NO3)2 đem đi nhiệt phân là 1,25 (g)
Bài 1 :
Sửa đề : Nung 17,6g hỗn hợp chất rắn X gồm NaHCO3 và Na2CO3 đến khối lượng không đổi thu được V lít khí hỗn hợp B gồm hơi và khí. Cho hỗn hợp khí hấp thụ hoàn toàn vào Ca(OH)2 dư thì được 12,5g khối lượng kết tủa. Tính thể tích khí và hơi trong V lít hỗn hợp B.
----------------------------------------------------Bài làm---------------------------------------------------------------------
Vì Na2CO3 bền nhiệt nên khi nung nóng sẽ không bị phân hủy
Ta có :
PTHH nung nóng NaHCO3 :
\(2NaHCO3-^{t0}\rightarrow Na2CO3+CO2+H2O\)
Hỗn hợp B thu được bao gồm : H2O (hơi ) và CO2(khí)
Ta có PTHH khi Cho hỗn hợp khí hấp thụ hoàn toàn vào Ca(OH)2 dư :
\(CO2+Ca\left(OH\right)2\rightarrow CaCO3\downarrow+H2O\)
0,125mol..........................0,0125mol
Kết tủa thu được là CaCO3 => mCaCO3=12,5 => nCaCO3=\(\dfrac{12,5}{100}=0,125\left(mol\right)\)
=> \(\left\{{}\begin{matrix}VH2O=0,125.2.22,4=5,6\left(l\right)\\VCO2=0,125.22,4=2,8\left(l\right)\end{matrix}\right.\)
Vậy..............