Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\Delta_rH^o_{298}=2\left(-825,5\right)+8\left(-296,8\right)-4\left(-177,9\right)\\ \Delta_rH^o_{298}=-3313,8\left(kJ\right)\)

2Na(s) + ½ O2(g) → Na2O(s) ${\Delta _f}H_{298}^0 = - 417,98$kJ.mol-1
Na(s) + ¼ O2(g) → ½ Na2O(s) ${\Delta _f}H_{298}^0 = \frac{{ - 417,98}}{2} = 208,99$kJ.mol-1

\(\Delta_rH^{^o}_{298}=945+494-2\cdot607=+225kJ\\ \Rightarrow D\)
Bạn ơi, bạn có biết gì về Eb không vậy? Mình tính Eb(cđ) - Eb(sp) mà? Công thức đó đâu ra vậy?

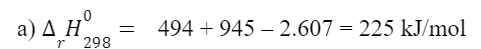
b) Trong N2, liên kết giữa 2 nguyên tử là liên kết ba – một loại liên kết bển, cần 1 năng lượng rất lớn để phá vỡ liên kết đó.
=> N2 khá trơ về mặt hóa học và chỉ phản ứng với oxy khi có nhiệt đô cao hoặc có tia lửa điện

nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)
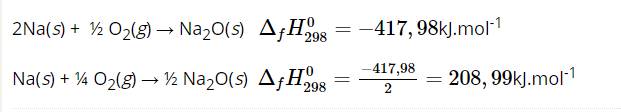
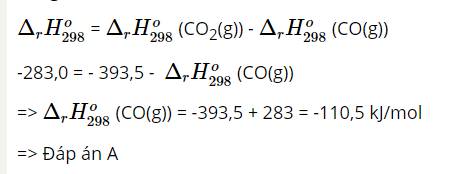
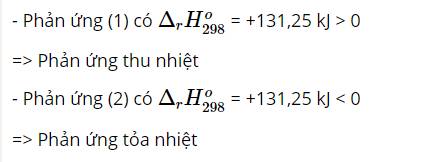
\(179,2.\dfrac{280000}{40+12+16.3}=501760kJ\)