Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(C\%=\dfrac{40}{100+40}.100\%=28,6\%\)
\(m_{muoian}=1000.28,6\%=286\left(g\right)\)
C% = \(\dfrac{40}{100+40}.100\%=28,6\%\)
=> mmuối = 1000 . 28,6% = 286 g

NaBr + AgNO3 \(\rightarrow\)AgBr + NaNO3
NaCl + AgNO3 \(\rightarrow\) AgCl + NaNO3
\(C_M=0,5M\Rightarrow n_{AgNO_3}=0,025\left(mol\right)\)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
\(\Rightarrow x=9,0557.10^{-3};y=0,01594\)
\(\Rightarrow C\%=\frac{0,594.58,5}{50}.100\%=1,865\%\)
NaBr + AgNO3 →→AgBr + NaNO3
NaCl + AgNO3 →→ AgCl + NaNO3
CM=0,5M⇒nAgNO3=0,025(mol)CM=0,5M⇒nAgNO3=0,025(mol)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
⇒x=9,0557.10−3;y=0,01594⇒x=9,0557.10−3;y=0,01594
⇒C%=0,594.58,550.100%=1,865%⇒C%=0,594.58,550.100%=1,865%

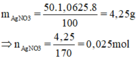
Phương trình hóa học của phản ứng:
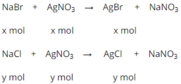
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số: 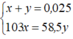
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
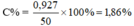

Chọn đáp án A
m d d A g N O 3 = V.D = 50.1,0625 = 53,125 (gam)
ð m A g N O 3 = 53 , 125 . 8 100 = 4,25 (gam) => n A g N O 3 = 4 , 25 170 = 0,025 (mol)
Nồng độ % của 2 muối bằng nhau => Khối lượng 2 muối bằng nhau.
N a C l : x m o l N a B r : y m o l → x + y = 0 , 025 58 , 5 x = 103 y → x = 0 , 0159 y = 0 , 0091
ð
C
%
N
a
C
l
=
0
,
0159.58
,
5
50
.100% = 1,86%

=
= 0, 025 mol
Phương trình hóa học của phản ứng:
NaBr + AgNO3 → AgBr↓ + NaNO3
X mol x mol x mol
NaCl + AgNO3 → AgCl↓ + NaNO3
Y mol y mol y mol
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Ta có hệ phương trình đại số:
Giải ra , ta có x = 0, 009 mol NaBr
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
C% = x 100% = 1,86%

\(n_{N_2}=\dfrac{0,224}{22,4}=0,01mol\\ 5Mg+12HNO_3\rightarrow5Mg\left(NO_3\right)_2+N_2+6H_2O\\ n_{Mg\left(NO_3\right)_2}=n_{Mg}=0,01.5=0,05mol\\ m_{Mg\left(NO_3\right)_2}=0,05.148=7,4g\\ n_{HNO_3}=0,01.12=0,12mol\\ m_{ddHNO_3}=\dfrac{0,12.63}{20\%}\cdot100\%=37,8g\\ m_{ddMg\left(NO_3\right)_2}=0,05.24+37,8-0,01.28=38g\\ C_{\%Mg\left(NO_3\right)_2}=\dfrac{7,4}{38}\cdot100\%=19,47\%\)

mk là mẫu bài 1 nha!!!!!!!!! có gì k đúng mong bạn đừng gạch đá
Ta có: \(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có \(n_{Zn}=2n_{HCl}\Rightarrow n_{HCl}=0,4\left(mol\right)\)
a,Ta có \(CM_{HCL}=\dfrac{n}{V}\Rightarrow V=\dfrac{n}{CM}=\dfrac{0,4}{0,5}=0,8\left(l\right)\)
b,\(n_{H_2}=\dfrac{V}{22.4}\Rightarrow V=0.2\times22.4=4.48\left(l\right)\)
c,\(C\%_{ZnCl_2}=\dfrac{m_{ct}}{m_{dd}}=\dfrac{0.2\times\left(65+71\right)}{0.8\times1000}\times100=3.4\%\)
đây là bài 1. mk chỉ nghĩ thế thôi chứ câu c vẫn k chắc lắc. có j pm nha
