Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tóm tắt: 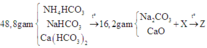
Gọi a; b; c lần lượt là số mol của NH4HCO3, NaHCO3 và Ca(HCO3)2
Ta có: 89a + 84b + 162c =48,8 (l)
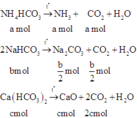
Khối lượng của hỗn hợp rắn là: 53b + 56c = 16,2 (2)
Hỗn hợp khí X gồm NH3 (a mol) và CO2 (a + b 2 + 2c)
⇒ n x = (2a + b 2 + 2c)
Khi X ở nhiệt độ 180 – 200°C, dưới áp suất khoảng 200 atm thì đây chính là phản ứng điều chế đạm urê nên ta có phản ứng:
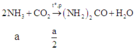
NH3 phản ứng với CO2 theo tỉ lệ 1:2 lượng khí Z còn lại chính là CO2 ⇒ n z = a 2 + b 2 . 2 c
Do sau phản ứng đưa về nhiệt độ ban đầu nên ta có:
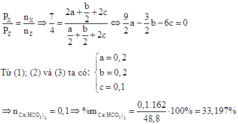
Đáp án A.

0,54 = 108x => x = 0,005 mol
=> mCu (NO3)2 = 0,94 g

Chọn đáp án C
m C a C O 3 = 0 , 8 m
C a C O 3 ® CaO + C O 2
a a a (mol)
44a = m – 0,78m Þ a = 0,005m
H % = 100 . 0 , 005 m . 100 % 0 , 8 m = 62 , 5 %

giả sử m CaCO3 = 100 g => nCaCO3 = 1mol
CaCo3 => CaO + CO2
m chất rắn giảm = mCO2
100.10% = 44x
=> x= 5/22 mol
=> %CaCO3 pư = \(\frac{\frac{5}{22}}{1}.100\%=22,73\%\)